
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 甲醇是一种优质燃料,可制作燃料电池.
甲醇是一种优质燃料,可制作燃料电池.查看答案和解析>>
科目: 来源: 题型:
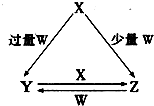 X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(水及部分产物已略去).
X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(水及部分产物已略去).
查看答案和解析>>
科目: 来源: 题型:
 的催化氧化
的催化氧化查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
 Ⅰ、将0.1g MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示.解释反应速率变化的原因:
Ⅰ、将0.1g MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示.解释反应速率变化的原因:查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
| A、5 | B、4 | C、3 | D、2 |
查看答案和解析>>
科目: 来源: 题型:
A、标准状况下,密度为dg/L的某气体纯净物一个分子的质量为
| ||
| B、1 mol FeCl3跟水反应完全转化成氢氧化铁胶体后,生成胶体粒子的数目为NA | ||
| C、31g白磷分子中,含有的共价单键数目是NA个 | ||
| D、电解CuCl2溶液时,若有NA个电子通过,则阴极增重64g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com