
科目: 来源: 题型:
| A、在标准状态下,2.24L己烷含有的氢原子数目为1.4NA |
| B、1.6g甲烷完全燃烧生成二氧化碳和水,转移的电子数为0.8NA |
| C、14g乙烯和环丙烷混合物中含有的碳原子数目为NA |
| D、0.1mol乙炔分子中含有的共用电子对数目为0.5NA |
查看答案和解析>>
科目: 来源: 题型:
| A、标准状况下,22.4L CO2和O2混合气体中含有的氧原子数约为NA |
| B、300mL 2mol?L-1蔗糖溶液中所含分子数为0.6NA |
| C、1L 1mol?L-1的K2CO3溶液中离子总数大于3NA |
| D、常温常压下,2.24 L四氯化碳中所含氯原子数约小于0.4NA |
查看答案和解析>>
科目: 来源: 题型:
| A、标准状况下,22.4L二氯甲烷的分子数为NA |
| B、常温常压下,2.0gD2气体分子含有的中子数为NA |
| C、100mL 1mol/L AlCl3溶液中所含阳离子数大于0.1NA |
| D、用石灰乳完全吸收1mol Cl2时,转移电子的数目是NA |
查看答案和解析>>
科目: 来源: 题型:
| A、25℃时,饱和AgCl溶液与饱和AgBr溶液相比,后者的c(Ag+)较大 |
| B、25℃时,若向AgBr的饱和溶液中加入少量AgCl的固体,则c(Br-)将减小 |
| C、25℃时,向饱和AgCl水溶液中加入NaCl溶液,Ksp[AgCl]将变大 |
| D、25℃时,在AgBr的悬浊液中加入NaCl溶液后,AgBr不可能转化为AgCl |
查看答案和解析>>
科目: 来源: 题型:
| A、0.22mol |
| B、0.24mol |
| C、0.52mol |
| D、0.65mol |
查看答案和解析>>
科目: 来源: 题型:
A、以石墨为电极电解MgCl2溶液:2Cl-+2H2O
| ||||
| B、NH4Cl水溶液显酸性:NH4++H2O═NH3?H2O+H+ | ||||
| C、AlCl3溶液中投入过量Na:Al3++4Na+2H2O═AlO2-+4Na++2H2↑ | ||||
| D、FeBr2溶液中通入少量Cl2:2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl- |
查看答案和解析>>
科目: 来源: 题型:

2- 3 |
查看答案和解析>>
科目: 来源: 题型:
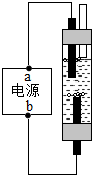 去年5月12日四川汶川发生发生特大地震后为防止灾后疫病使用了大量的各种消毒液,如NaClO溶液.某学习小组对消毒液次氯酸钠(NaClO)的制备与性质进行研究.
去年5月12日四川汶川发生发生特大地震后为防止灾后疫病使用了大量的各种消毒液,如NaClO溶液.某学习小组对消毒液次氯酸钠(NaClO)的制备与性质进行研究.| 主要有效成分为次氯酸钠,有效氯含量8 000~10000 mg/L.可用于各类家居用品、 餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用.本品须密封,置阴凉暗处保存. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com