
科目: 来源:2014-2015湖南省怀化市小学课改高二上学期期末化学试卷(解析版) 题型:选择题
用惰性电极电解一定量的硫酸铜溶液,当转移0.4 mol电子时,阴极开始产生气体,继续电解又转移0.2 mol电子时停止电解。下列说法正确的是
A.电解过程中,溶液的pH不断增大
B.当转移0.4 mol 电子时,电解生成的铜为12.8 g
C.阴极反应式为2H2O+4e-=4H++O2↑
D.整个过程中产生的H2与O2的体积比为2:1
查看答案和解析>>
科目: 来源:2014-2015湖南省怀化市小学课改高二上学期期末化学试卷(解析版) 题型:实验题
(每空2分,共16分)
Ⅰ、中学化学实验中的中和热的测定实验常用0.50 mol·L-1 HCl和0.55 mol·L-1的NaOH溶液各50 mL。NaOH的浓度大于HCl的浓度作用是___________。在大小烧杯之间填满碎泡沫(或纸条)其目的是: 。
Ⅱ、某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选甲基橙作指示剂。
(1)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_____________。直到因加入一滴盐酸后,溶液由黄色变为橙色,并______________________________为止。
(2)若滴定前平视读数,滴定终点时俯视读数,则会使所测NaOH溶液的浓度 。(填“无影响”、“偏高”或“偏低”)。
Ⅲ、用实验确定某酸HA是弱酸。两同学的方案是:
甲:①配制0.1 mol·L-1的HA溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱酸。
乙:①配制0.1 mol·L-1的HA溶液100 mL;配制0.1 mol·L-1的盐酸溶液100 mL
②取相同体积的0.1 mol·L-1的HA和0.1 mol·L-1的盐酸溶液分别装入两只试管,同时加入表面积大小相同的锌粒,观察现象,即可证明HA是弱酸。
(1)在两个方案的第①步中,都要用到的定量仪器是____________________。
(2)甲方案中,说明HA是弱酸的理由是测得溶液的pH______ 1(选填“>”、“<”或“=”);乙方案中,说明HA是弱酸的现象是_______。
a.装HCl溶液的试管中放出H2的速率快
b.装HA溶液的试管中放出H2的速率快
c.两只试管中产生气体速率一样快
查看答案和解析>>
科目: 来源:2014-2015湖南省怀化市小学课改高二上学期期末化学试卷(解析版) 题型:填空题
(每空2分,共14分)电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
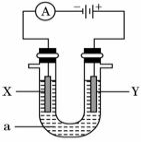
(1)若X、Y都是惰性电极,a是饱和KCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则①Y电极上的电极反应式为____________________,该电极产生的现象是 。
②该反应的总反应化学方程式是: ______________________________________________。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是__________,电极反应式是____________________。
(3)若用惰性电极电解500 mL CuSO4溶液,溶液中 Cu2+ 完全电解后,停止电解,取出X电极,洗涤、干燥、称量,电极质量增加1.6 g。
①要使电解后溶液恢复到电解前的状态,需加入一定量的________(填加入物质的化学式)。(假设电解前后溶液的体积不变)
②溶液的pH= 。
查看答案和解析>>
科目: 来源:2014-2015湖南省怀化市小学课改高二上学期期末化学试卷(解析版) 题型:填空题
(每空2分,共12分)
I、(1)已知1 g H2S气体完全燃烧,生成液态水和二氧化硫气体,放出17.24 kJ热量,请写出H2S气体燃烧热的热化学方程式:
(2)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4 mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256.652KJ的热量。反应的热化学方程式为 。
II、已知常温下在NaHSO3溶液中c(H2SO3 )<c(SO32 -) 且H2SO3 的电离平衡常数为: K1=1.5×10-2 K2=1.1×10-7 ;氨水的电离平衡常数为K=1.8×10-2 ;
(1)则等物质的量浓度的下列五种溶液:①NH3·H2O ②KHSO3 ③KHCO3 溶液中水的电离程度由大到小排列顺序为
(2)0.1 mol·L-1的NaHSO3溶液中C(H+) C(OH-)(“>”、“<”或“=”):
Ⅲ、已知25 ℃时Ksp[Mg(OH)2]=5.6×10-12,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.1×10-33
(1)在25 ℃下,向浓度均为0.1 mol/L的AlCl3和CuCl2混合溶液中逐滴加入氨水,先生成________沉淀(填化学式)。
(2)溶液中某离子物质的量浓度低于1.0×10-5 mol/L时,可认为已沉淀完全。现向一定浓度的AlCl3和FeCl3的混合溶液中逐滴加入氨水,当Fe3+完全沉淀时,测定c(Al3+)=0.2 mol/L。此时所得沉淀中________(填“含有”或“不含有”)Al(OH)3。
查看答案和解析>>
科目: 来源:2014-2015湖南省怀化市小学课改高二上学期期末化学试卷(解析版) 题型:填空题
(每空2分,共16分)
I、恒温下,将a mol N2与b mol H2的混合气体通入一个固体容积的密闭容器中,发生如下反应:
N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)该反应的平衡常数表达式为:K=
(2)若反应进行到某时刻t时,nt(N2)=8 mol,nt(NH3)=4 mol,计算 a= 。当反应达到平衡时,混合气体的体积为537.6 L(标况下),其中NH3的含量(体积分数)为25%。原混合气体中, a:b= 。
Ⅱ、反应mA+nB pC+qD在某温度下达到平衡。
pC+qD在某温度下达到平衡。
①若A、B、C 、D都是气体,保持温度不变,将气体体积压缩到原来的一半,当再次达到平衡时C的物质的量浓度变为原来的1.6倍,则m、n、p、q的关系是m+n p+q(填“<”或“>”或“=”) 。
②若A、B、C ,D都为气体,且m+ n = p+q,则将气体体积压缩后A的物质的量将 _________(填“减小”“增大”“不变”),平衡______移动。(填“正向”或“逆向”或“不”)
③若给体系升温,B的物质的量减少,则正反应为 ________反应(填“放热”或“吸热”)
④若在体系中增加A的量,平衡不发生移动,则A肯定不能为_____态。
查看答案和解析>>
科目: 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.化学反应一定有物质变化,不一定有能量变化
B.化合反应一定是放热反应
C.放热反应不需要加热就一定能发生
D.吸热反应不加热也可能发生
查看答案和解析>>
科目: 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
下列属于放热反应的是
A.浓硫酸的稀释 B.铝热反应
C.氢气还原氧化铜 D.Ba(OH)2·2H2O和NH4Cl(固体)混合
查看答案和解析>>
科目: 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
下列水溶液一定呈中性的是
A.pH=7的溶液
B.c(H+)=1.0×10-7mol·L-1的溶液
C.c(H+) =c(OH-)
D.pH=3的酸与pH=11的碱等体积混合后的溶液
查看答案和解析>>
科目: 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
在理论上不能用于设计原电池的化学反应是
A.NaCl(aq)+ AgNO3(aq)= AgCl(s)+ NaNO3(aq )△H<0
B.2CH3OH (l) +3O2 (g) = 2CO2 (g) + 4H2O (l)△H<0
C.2FeCl3(aq)+Fe(s) = 3FeCl3(aq) △H < 0
D.2H2 (g) + O2 (g) = 2H2O (l) △H < 0
查看答案和解析>>
科目: 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
工业制硫酸时有一反应为:2SO2+O2 2SO3。对该反应的有关说法错误的是
2SO3。对该反应的有关说法错误的是
A.该反应是可逆反应 B.反应中SO2能全部转化为SO3
C.催化剂能加快该反应的速率 D.升高温度能加快该反应的速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com