
科目: 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:填空题
(12分)黄钾铵铁矾[KNH4Fex(SO4)y(OH)z]不溶于水和稀硫酸,制取黄钾铵铁矾的流程如下:

(1)溶液X是 。
(2)检验滤液中是否存在K+的操作是 。
(3)黄钾铵铁矾的化学式可通过下列实验测定:
①称取一定质量的样品加入稀硝酸充分溶解,将所得溶液转移至容量瓶并配制成100.00 mL溶液A。
②量取25.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体9.32 g。
③量取25.00 mL溶液A,加入足量NaOH溶液,加热,收集到标准状况下气体224mL,同时有红褐色沉淀生成。
④将步骤③所得沉淀过滤、洗涤、灼烧,最终得固体4.80 g。
通过计算确定黄钾铵铁矾的化学式(写出计算过程) 。
查看答案和解析>>
科目: 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:实验题
(14分)某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。请填写下列空白:
Ⅰ.测定过氧化氢的含量
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250 mL_______(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00 mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式为________。
(3)判断滴定到达终点的现象是_________________________。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为____________。
(5)若滴定前滴定管尖嘴中有气泡,滴定后气泡消失,则测定结果_________(填“偏高”或“偏低”或“不变”)。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾淀粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)
请将他们的实验方法和实验现象填入下表:
实验内容 | 实验方法 | 实验现象 |
验证氧化性 | ||
验证不稳定性 |
查看答案和解析>>
科目: 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:填空题
(15分)研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下放热反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 ?H =a kJ/mol (I)
NaNO3(s)+ClNO(g) K1 ?H =a kJ/mol (I)
2NO(g)+Cl2(g) 2ClNO(g) K2 ?H =b kJ/mol (II)
2ClNO(g) K2 ?H =b kJ/mol (II)
(1)反应4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示),?H= kJ/mol(用a、b表示)。
2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K= (用K1、K2表示),?H= kJ/mol(用a、b表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。测得10min内v(ClNO)=7.5×10-3mol?L-1?min-1,则平衡后
n(Cl2)= mol。其它条件保持不变,反应(II)在恒压条件下进行,平衡常数K2 (填“增大”“减小”或“不变”)。
(3)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol?L?1的CH3COONa溶液,则两溶液中c(NO3?)、c(NO2-)和c(CH3COO?)由大到小的顺序为 。(已知HNO2的电离常数Ka=7.1×10-4mol?L?1,CH3COOH的电离常数K a=1.7×10-5mol?L?1)
(4)由有机阳离子、Al2Cl7—和AlCl4—组成的离子液体作电解液时,可在钢制品上电镀铝。
钢制品应接电源的 极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为 。若改用AlCl3水溶液作电解液,则阴极产物为 。
查看答案和解析>>
科目: 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:填空题
(12分)氮元素可形成氢化物、卤化物、氮化物、叠氮化物和配合物等多种化合物。
(1)肼(N2H4)可用作火箭燃料,其原理是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g),若反应中有4mol N-H 键断裂,则形成的π键有 mol。
(2)F2和过量NH3在铜催化作用下反应生成NF3,NF3分子的空间构型为 。
(3)铁和氨气在640℃发生置换反应,产物之一的晶胞见图1。该反应的化学方程式: 。
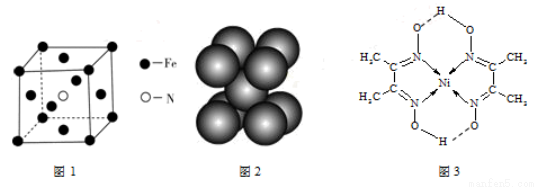
(4)叠氮化钠(NaN3)分解反应为:2NaN3(s)=2Na(l)+3N2(g),下列有关说法正确的是 。
a.常温下N2很稳定,是因为N的电负性大
b.钠晶胞见图2,每个晶胞含有2个钠原子
c.第一电离能(I1):N>O>S
d.NaN3与KN3结构类似,晶格能:NaN3<KN3
(5)配合物Y的结构见图3,Y中含有 (填序号);
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
Y中碳原子的杂化方式有 。
查看答案和解析>>
科目: 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:选择题
化学与社会、生活密切相关,下列说法不正确的是
A.在食品袋中放入盛有CaO和硫酸亚铁的透气小袋,可防止食物受潮、氧化变质
B.MgO、Al2O3的熔点很高,工业上用于制作耐高温材料,也用与冶炼铝和镁
C.发酵粉中主要含有碳酸氢钠,能使焙制出的糕点疏松多孔
D.利用ClO2对自来水消毒主要是因为ClO2具有强氧化性
查看答案和解析>>
科目: 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:选择题
能用如图气体制取装置制取少量气体并能“随开随用、随关随停”的是

A.大理石和稀硫酸制取二氧化碳
B.锌粒和稀硫酸制氢气
C.浓盐酸和二氧化锰制取氯气
D.过氧化钠和水制取氧气
查看答案和解析>>
科目: 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数,下列说法正确的是
A.500mL2mol/L葡萄糖溶液中所含分子数为NA
B.0.1mol/L Na2CO3溶液中的阴离子总数大于0.1NA
C.电解精炼铜时,若阳极质量减少64g,则外电路导线上不一定通过2NA个电子
D.5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA
查看答案和解析>>
科目: 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:选择题
下列各组离子能在指定溶液中大量共存的是
①无色溶液中:Al3+、Cl-、Na+、HCO3-、SO42-
②pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
③加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
④使pH试纸呈红色的溶液中:Fe3+、MnO4-、Na+、SO42-
⑤酸性溶液中:Fe2+、Al3+、NO3-、I-
A.①②④ B.①⑤ C.②③④ D.①②③
查看答案和解析>>
科目: 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:选择题
如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1 mol,水的质量为100 g.。

下列说法正确的是
A.Na2O2晶体中阴阳离子数目之比为1∶1
B.反应③最多能产生0.05 mol O2
C.反应①的离子方程式为Na+2H2O==Na++2OH-+H2↑
D.①、②、③充分反应后所得溶液的质量分数从大到小的顺序为①>②>③
查看答案和解析>>
科目: 来源:2014-2015学年宁夏银川市高三上学期期末理综化学试卷(解析版) 题型:选择题
短周期主族元素X、Y、Z、M、W在元素周期表中的相对位置如图,其中Z的核电荷数是Y 的两倍.下列说法正确的是
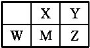
A.M位于元素周期表中第三周期ⅣA族
B.原子半径:Z>M>X
C.气态氢化物的热稳定性:Y>X>W
D.W的氧化物既能与NaOH反应,也能与HF反应,属于两性氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com