
科目: 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:选择题
常温下,向饱和氯水中逐滴滴入0.1mol·L-1的氢氧化钠溶液,pH变化如下图所示,下列有关叙述正确的是
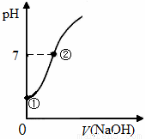
A.①点所示溶液中只存在HClO的电离平衡
B.②点所示溶液中:c(Na+)=c(Cl-) + c(ClO-)
C.I-能在②点所示溶液中存在
D.①到②水的电离程度逐渐减小
查看答案和解析>>
科目: 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:选择题
正、负极都是碳材料的双碳性电池,电池充、放电过程为2nC+LiA  CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
CnA+LiCn,充电时Li+、A-分别吸附在两极上形成LiCn和CnA(如图所示),下列说法正确的是
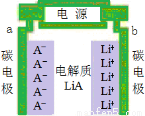
A.a是电池的负极
B.放电时,A-离子向b极移动
C.放电时,负极的电极反应式是nC-e-+A-= CnA
D.充电时,电解质中的离子浓度保持不变
查看答案和解析>>
科目: 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:填空题
(7分)用如图所示装置做“铜与浓硝酸反应”的实验。

(1)从试剂瓶中取出一小块铜片放入试管中,需用的仪器是 。
(2)棉花应蘸 溶液(填化学式)。
(3)试管中除了溶液变成绿色外,还会出现的现象是 (填序号)。
A.有红棕色气体生成,上下颜色相同
B.有红棕色气体生成,上部颜色较浅
C.有红棕色气体生成,下部颜色较浅
(4)实验结束后,对试管内残留物的处理方法是 。
查看答案和解析>>
科目: 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:实验题
(11分)果汁在生产过程中添加亚硫酸及其盐类,以抑制有害微生物的生长及抗氧化。某化学兴趣小组查阅文献后,用下图所示装置测定某果汁样品中SO2残留量。
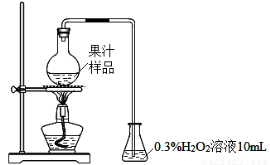
实验步骤:
(ⅰ)在烧瓶中加入50.00 mL果汁样品与3mL浓硫酸的混合液,加热10 min。
(ⅱ)移出锥形瓶,迅速滴入2~3滴酚酞试液,用0.01000 mol·L-1NaOH标准溶液滴定。
回答问题:
(1)实验室配制NaOH标准溶液时,不需要用到的仪器是 。
A.容量瓶 B.胶头滴管 C.烧瓶 D.玻璃棒
(2)将50. 00 mL果汁样品与3mL浓硫酸混合的操作是 。
(3)锥形瓶中发生反应的离子方程式是 。
(4)若步骤(ⅱ)消耗NaOH标准溶液25. 00 mL,则果汁样品中SO2残留量是 g/L。
(5)若改用0.5%的碘水10 mL作吸收液,实验中消耗NaOH标准溶液体积 。
A.V = 25 mL B.25 mL<V<50 mL C.V>50 mL
查看答案和解析>>
科目: 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:填空题
(9分)4种短周期元素相对位置如下表。M元素既是构成生物体的基本元素,又是构成地壳中岩石和化石燃料的主要元素。回答下列问题:

(1)X的原子结构示意图为 。
(2)0.1 molQ的10电子氢化物与CuO反应生成Cu2O、H2O和Q单质时,生成Cu2O的物质的量是 。
(3)Y的氧化物与NaOH溶液反应的化学方程式是 。
(4)HR是含M元素的一元酸。常温下,0.1 mol·L-1 HR 溶液中,c(H+) = 1.3×10-3 mol·L-1。则HR  H++R-的电离平衡常数Ka= (保留一位小数)。
H++R-的电离平衡常数Ka= (保留一位小数)。
查看答案和解析>>
科目: 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:填空题
(8分)以钛酸亚铁(FeTiO3)为原料制取BaTiO3的过程如下图所示:

(1)FeTiO3与稀硫酸反应,产物有TiOSO4、H2O和 (填化学式)。
(2)已知:TiO2(s)+H2SO4(aq)=TiOSO4(aq)+H2O (l) △H=a kJ·mol-1
H2TiO3(s)=TiO2(s)+H2O (l) △H=b kJ·mol-1
写出TiOSO4水解生成H2TiO3的热化学方程式 。
(3)写出TiO2生成BaTiO3的化学方程式 。
查看答案和解析>>
科目: 来源:2014-2015学年福建省宁德市高三上学期期末化学试卷(解析版) 题型:简答题
(20分)硝酸铝是重要的化工原料。
(1)在实验室中,硝酸铝必须与可燃物分开存放,是因为硝酸铝具有 。
A.可燃性 B.氧化性 C.还原性
(2)用Al作电极电解HNO3溶液制取Al(NO3)3,电解反应的离子方程式为 。
(3)查资料得知:当Al(NO3)3溶液pH>3时,铝元素有多种存在形态,如Al3+、[Al(OH)]2+、[Al(OH)2]+等。写出[Al(OH)]2+转化为[Al(OH)2]+的离子方程式 。
(4)用硝酸铝溶液(加入分散剂)制备纳米氧化铝粉体的一种工艺流程如下。

①(CH2)6N4水溶液显碱性。请补充完整下列离子方程式。

②经搅拌Ⅱ,pH下降的原因是 。
③凝胶中含有的硝酸盐是 。
(Ksp[Al(OH)3] =1.3×10-33 ;溶液中离子浓度小于1×10-5 mol·L-1时,可认为这种离子在溶液中不存在)
④煅烧过程主要发生如下转化: 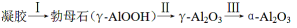 。
。
煅烧过程中样品的失重率(TG%)随温度变化如图。凝胶煅烧失重曲线有明显的三个阶段:

(i)a~b段:失重率82.12%;
(ii)b~c段:失重率9.37%;
(iii)c~d段:失重率几乎为0;
转化Ⅱ对应的失重阶段是 (填序号),转化Ⅲ开始的温度是 。
查看答案和解析>>
科目: 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
与社会、生产、生活、环境等密切相关,下列说法正确的是
A.氟利昂作制冷剂会加剧雾霾天气的形成
B.计算机芯片的材料是二氧化硅
C.汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的
D.利用二氧化碳制造全降解塑料,可以缓解温室效应
查看答案和解析>>
科目: 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
下列有关物质分类说法正确的是
A.钠、镁、铁对应的氧化物都是碱性氧化物
B.食醋、纯碱、食盐分别属于酸、碱、盐
C.生铁、不锈钢、青铜都属于合金
D.明矾、小苏打、水玻璃、次氯酸均为电解质
查看答案和解析>>
科目: 来源:2014-2015学年福建省等三校高三上学期联考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.HClO的结构式:H—Cl—O
B.氨气分子的比例模型
C.原子核内有10个中子的氧原子:
D.H2与H+互为同位素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com