
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:选择题
要证明CuSO4溶液显蓝色不是由于SO42-造成的,下列实验无意义的是
A.观察K2SO4溶液的颜色
B.加水稀释CuSO4溶液,溶液颜色变浅
C.向CuSO4溶液中滴加过量NaOH溶液,振荡后静置,溶液变成无色
D.向CuSO4溶液中滴加过量Ba(NO3)2溶液,振荡后静置,溶液未变成无色
查看答案和解析>>
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:选择题
下列实验事实得出的结论不正确的是
选项 | 实验事实 | 结论 |
A | H2可在Cl2中燃烧 | 燃烧不一定有氧气参加 |
B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 氧化铝熔点高于铝 |
C | 将SO2通入含HClO的溶液中,生成H2SO4 | HClO酸性比H2SO4强 |
D | 向FeCl2溶液中滴入KSCN溶液,在液面出现微红色 | Fe2+在空气中被氧化 |
查看答案和解析>>
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:选择题
某抗酸药的有效成分是碱式碳酸镁铝[AlMg3(OH)7CO3],将碱式碳酸镁铝溶于过量盐酸中,产生无色气体A和无色溶液B。下列说法不正确的是
A.A为CO2
B.AlMg3(OH)7CO3与盐酸的反应属于复分解反应
C.AlMg3(OH)7CO3与消耗的H+的物质的量之比为1:9
D.向溶液B中逐滴加入NaOH溶液至过量,产生的白色沉淀最终完全溶解
查看答案和解析>>
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:选择题
粗盐中含有不溶性泥沙,可溶性的CaCl2、MgCl2以及一些硫酸盐等。精制食盐水的实验操作顺序如下:①加入过量BaCl2溶液,②加入过量NaOH溶液,③加入过量Na2CO3溶液,④加入适量盐酸,⑤过滤。下列说法不正确的是
A.①②③中加入过量的试剂是为了完全除去相应的杂质离子
B.③中加入过量Na2CO3溶液仅为了完全除去Ca2+
C.因为Mg(OH)2难溶而MgCO3微溶,所以用NaOH除Mg2+效果比用Na2CO3好
D.④中可以通过边滴加边测定溶液pH的方法,控制加入的盐酸“适量”
查看答案和解析>>
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:填空题
H2O2是重要的化工原料。
(1)H2O2中O元素的化合价为______。
(2)①向酸性KMnO4溶液中滴加H2O2溶液,溶液褪色,体现了H2O2的还原性,其中氧化过程是:H2O2→______(填化学式)。
②向H2SO4酸化的FeSO4溶液中滴加H2O2溶液,溶液变成黄色,体现了H2O2的氧化性,反应的离子方程式是_________。
(3)H2O2不稳定易分解。实验室需要448 mL O2(标准状况),则理论上最少需要用30%的H2O2溶液(密度为1.10 g/mL)_______mL。(计算结果保留一位小数)
查看答案和解析>>
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:实验题
电子工业中用过量的FeCl3溶液溶解电路板中的铜箔时,会产生大量废液。由该废液回收铜并得到净水剂(FeCl36H2O)的步骤如下:
(2)I中加入过量Fe粉 ,然后过滤,滤渣中有Cu、Fe,为了得到纯净铜,不产生新的杂质,试剂A应是HCl。.在废液中加入过量铁粉,过滤;
II.向I的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
III.合并I和II中的滤液,通入足量氯气;
IV.……,得到FeCl36H2O晶体。
(1)用FeCl3溶液腐蚀铜箔的离子方程式是 。
(2)试剂A是 。
(3)取少量步骤III所得的溶液于试管中,能够证明通入氯气足量的是 。
a.检验Cl2的存在 b检验Fe3+的存在 c.检验Fe2+的不存在
(4)完成步骤IV需要用到的实验装置是 (填字母)。
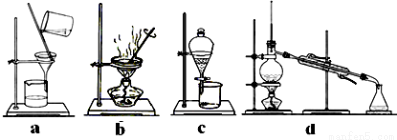
查看答案和解析>>
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:填空题
下图为氮及其化合物的类别与化合价对应的关系图。

(1)实验室制取氨气。
① 化学方程式是 。
② 可用向下排空气法收集氨气的原因是 。
③ 用水吸收多余的氨气时,如将导管直接插入水中,
会产生倒吸现象,产生该现象的原因是 。
(2)完成下列能生成NO的化学方程式:
① 体现N元素的还原性:
a. 汽车尾气中产生的NO:N2 + O2  2NO。
2NO。
b. 氨的催化氧化:_________。
② 体现N元素的氧化性:_________。
(3)NO2 易溶于水。将体积为V mL的试管充满NO2后倒扣在水中,见下图。

① NO2溶于水的化学方程式是_________。
② 使试管中NO2完全被水吸收的操作是________。
查看答案和解析>>
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:实验题
某小组同学通过对比实验了解Na2CO3和NaHCO3性质的异同,下表是他们撰写的实验报告的一部分。
实验序号 | 实验步骤(内容) | 现象 |
① | 在贴有标签a、b的试管中分别加入1.0 g Na2CO3固体和NaHCO3固体,观察外观。 | |
② | 分别滴入几滴水,振荡,摸试管底部。 | 试管 放热现象更明显(填“a”或“b”)。 |
③ | 继续向两试管中分别加入10.0 mL水,用力振荡,观察现象。 | |
④ | 再分别向两试管中滴加2滴酚酞溶液,观察现象。 | 溶液均变红,颜色较深的试管是_________(填“a”或“b”)。 |
⑤ | 最后分别向两溶液中滴加足量盐酸。 | 红色褪去,均有无色气体产生。经计算生成气体的量a_____b(填“>”“<”或“=”)。 |
⑥ | 加热大试管一段时间。(注:棉花球沾有无水硫酸铜粉末)
|
(1)请帮助该小组同学完成实验报告中的内容。
(2)已知:20℃时Na2CO3的溶解度为20.5 g。由实验 (填实验序号)现象可知,20℃时NaHCO3的溶解度小于20.5 g;如果向饱和Na2CO3溶液中不断通入CO2气体,现象是 ,化学方程式是 。
(3)由实验⑥可以得出的结论是 ,用化学方程式说明得出结论的原因 。
查看答案和解析>>
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:实验题
下图为铜丝与浓硫酸反应并验证其产物性质的实验装置。


(1)①中反应的化学方程式是 。其中铜发生了 (填“氧化”或“还原”)反应,判断依据为 。
(2)②中饱和NaHSO3溶液的作用是除去①中挥发出的硫酸。加热一段时间后,③中溶液依然澄清,④中溶液褪色。想要立即终止铜与硫酸的反应,最恰当的方法是 。
a.上移铜丝,使其脱离硫酸
b.撤去酒精灯
c.拔去橡胶塞倒出硫酸
(3)反应停止后,待装置冷却,把③取下后将其中溶液分成两份做如下实验:
加入试剂 | 现象 | 反应的离子方程式 | |
第一份 | 加入NaOH溶液 | 有白色沉淀生成 | ____________ |
第二份 | 加入氯水 | 有白色沉淀生成 | ____________ |
完成上述反应的离子方程式。
(4)④中棉花团的作用是 。
(5)上述实验结束后,发现①中试管内有少量白色固体出现,冷却后将试管中的物质缓缓倒入水中,溶液呈蓝色。取少量蓝色溶液于试管中,滴加NaOH溶液至过量,出现的现象是 。
查看答案和解析>>
科目: 来源:2014-2015北京市朝阳区高一上学期期末考试化学试卷(解析版) 题型:填空题
氯气及其相关产品在生活、生产中应用广泛。
(1)氯气属于有毒气体,在实验室进行相关实验时,除必须进行尾气处理外,还应注意的问题是 ;若在生活中遇贮氯罐意外泄漏,应 (填“顺风”或“逆风”)疏散,消防员喷洒稀NaOH溶液的作用是 。(用化学方程式表示)
(2)① 实验室常用NaOH溶液吸收多余的氯气,下列试剂也可用于吸收氯气的是 (填字母)。
a. NaCl溶液 b. FeSO4溶液 c. Na2SO3溶液
② 写出①中你选择的吸收试剂与Cl2反应的离子方程式: 。

(3)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如下图。

①分析“对金属制品有腐蚀作用”的原因 。
②需“密闭保存”的原因 。
③“与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式: 。
(4)若空气中氯气的含量超过0.1 mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗了0.001 mol/L的KI溶液 100 mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com