
科目: 来源: 题型:
下列溶液中离子一定能够大量共存的是( )
A. 加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+
B. 能使淀粉碘化钾试纸显蓝色的溶液中:K+、SO42-、S2-、SO32-
C. c(H+)∶c(OH-)=1∶1012的水溶液中:CO32-、Na+、NO3-、AlO2-
D. 无色溶液中:K+、Na+、MnO4-、SO42-
查看答案和解析>>
科目: 来源: 题型:
下列有关物质的性质和该性质的应用均正确的是( )
A.氨气具有氧化性,用浓氨水检验Cl2管道是否泄漏
B.氢氟酸具有强酸性,用氢氟酸蚀刻玻璃
C.碳酸氢钠热稳定性弱,用作焙制糕点的发酵粉
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
查看答案和解析>>
科目: 来源: 题型:
高分子材料E和含扑热息痛高分子药物的合成流程如下图所示:

已知:I.含扑热息痛高分子药物的结构为: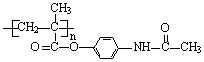 。
。
II.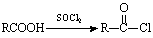
III.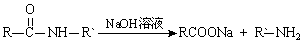
试回答下列问题:
(1)①的反应类型为____________,G的分子式为____________。
(2)若1 mol 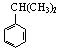 可转化为1 mol A和1 mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式______________。
可转化为1 mol A和1 mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式______________。
(3)反应②为加成反应,则B的结构简式为_______;扑热息痛的结构简式为__ __。
(4)D蒸气密度是相同状态下甲烷密度的6.25倍,D中各元素的质量分数分别为碳60%,氢8%,氧32% 。D分子中所含官能团为______________。
(5)写出含扑热息痛高分子药物与足量氢氧化钠溶液发生反应的化学方程式_________。
(6)D有多种同分异构体,其中与D具有相同官能团,且能发生银镜反应的同分异构体有_______种(考虑顺反异构)。
查看答案和解析>>
科目: 来源: 题型:
甲酸甲酯水解反应方程式为:
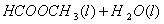 ≒
≒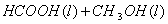
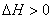
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始量如下表:

甲酸甲酯转化率在温度T1下随反应时间(t)的变化如下图:

(1)根据上述条件,计算不同时间范围内甲酸甲酯的平均反应速率,结果见下表:

请计算15-20min范围内甲酸甲酯的减少量为 mol,甲酸甲酯的平均反应速率
为 mol·min-1(不要求写出计算过程)。
(2)依据以上数据,写出该反应的反应速率在不同阶段的变化规律及其原因: 。
(3)上述反应的平衡常数表达式为: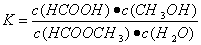 ,则该反应在温度
,则该反应在温度
T1下的K值为 。
(4)其他条件不变,仅改变温度为T2(T2大于T1),在答题卡框图中画出温度T2下甲酸甲酯转化率随反应时间变化的预期结果示意图。
查看答案和解析>>
科目: 来源: 题型:
用水处理金属钠与碳化钙的混合物,有气体放出,此气体在催化剂作用下恰好完全反
应,生成另一种气体A。气体A完全燃烧时,需要3.5倍体积的氧气,则金属钠与
碳化钙的物质的量之比是
A.2∶1 B.1∶2 C.4∶1 D.1∶4
查看答案和解析>>
科目: 来源: 题型:
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s)。
下列说法错误的是
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e- == Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过O.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写不正确的是
A.AlCl3溶液与烧碱溶液反应,当n(OH-):n(Al3+ )=7:2时:
2Al3+ + 7OH - = Al(OH)3↓+ AlO2- + 2H2O
B.氨水吸收足量的SO2气体:NH3·H2O+SO2=NH4+ + HSO3-
C.高锰酸钾酸性溶液与草酸溶液反应:
2MnO4-+ 5C2O42- + 16H+ = 2Mn2+ + 10CO2↑+ 8H2O
D.向Fe(OH)3悬浊液中加入氢碘酸:Fe(OH)3+3H+= Fe3++3H2O
查看答案和解析>>
科目: 来源: 题型:
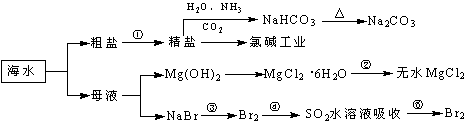
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
下列有关说法正确的是
A.制取NaHCO3的反应是利用其溶解度小于NaCl
B.用澄清的石灰水可鉴别NaHCO3和Na2CO3
C.在第③、④、⑤步骤中,溴元素均被氧化
D.工业上通过电解饱和MgCl2溶液制取金属镁
查看答案和解析>>
科目: 来源: 题型:
在一个可以加热的密闭容器中,加入Na2O2和NaHCO3各0.5mol,将容器加热至400℃,待充分反应后排出气体,则容器中剩余的固体是
A.Na2CO3 B.Na2CO3和Na2O2 C.NaOH D.Na2CO3和NaOH
查看答案和解析>>
科目: 来源: 题型:
已知酸式盐NaHB在水溶液中存在下列反应:
① NaHB=Na++HB-,② HB-≒H++B2-,③ HB-+H2O≒H2B+OH-且溶液中
c(H+)>c(OH-),则下列说法错误的是
A.NaHB为强电解质 B.NaHB溶液中:c(Na+) > c(HB-) +2c(B2-)
C.H2B为弱电解质 D.HB-的电离程度小于HB-的水解程度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com