
科目: 来源: 题型:
如下图所 示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是
示,△H1=-393.5 kJ•mol-1,△H2=-395.4 kJ•mol-1,下列说法或表示式正确的是

A.石墨和金刚石的转化是物理变化
B.1mol石墨的总能量比1 mol金刚石的总能量大1.9 kJ
C.金刚石的稳定性强于石墨
D.C(s、石墨)= C(s、金刚石) △H= +1.9 kJ•mol-1
查看答案和解析>>
科目: 来源: 题型:
在同温同压下,下列各组热化学方程式中,△H2>△H1的是
A.S(g)+O2(g)=SO2(g), △H1; S(s)+O2(g)=SO2(g), △H2
B.2H2(g)+O2(g)=2H2O(g),△H1; 2H2(g)+O2(g)=2H2O(l), △H2
C.C(s)+  O2(g)=CO(g)
O2(g)=CO(g)  △H1;C(s)+O2(g)=CO2(g) △H2
△H1;C(s)+O2(g)=CO2(g) △H2
D.H2(g)+Cl2(g)=2HCl(g),△H1; 2H2(g)+2Cl2(g)=4HCl(g),△H2
查看答案和解析>>
科目: 来源: 题型:
在压强为2.20×104 kPa、温度达到374℃时,水成为“超临界状态”,此时水可将CO2等含碳化合物转化为有机物,这就是“水热反应”,生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源。下列说法不正确的是( )
A.二氧化碳与超临界水作用生成汽油的反应,属于放热反应
B.“水热反应”是一种复杂的物理化学变化
C.火力发电厂可望利用废热,将二氧化碳转变为能源物质
D.随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环
查看答案和解析>>
科目: 来源: 题型:
某化学活动小组设计如下图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质。

(1)写出装置A中发生反应的离子方程式:
(2)写出试剂Y的名称:_____________________。
(3)已知:通入一定量的氯气后,测得D中只有一种常温下为黄红色的气体,其为含氯氧化物。可以确定的是C中含有的氯盐只有一种,且含有NaHCO3,现对C成分进行猜想和探究。
①提出合理假设:
假设一:存在两种成分: NaHCO3和__________
假设二:存在三种成分: NaHCO3和__________、___________。
②设计方案,进行实验。请写出实验步骤以及预期现象和结论(可不填满)。
限选实验试剂和仪器:蒸馏水、稀硝酸、BaCl2溶液、澄清石灰水、AgNO3溶液、试管、小烧杯。
| 实验步骤 |
|
| 步骤1:取C中的少量固体样品于试管中,滴加 足量蒸馏水至固体溶解,然后将所得溶液分别置于A、B试管中。 | |
| 步骤2:向A试管中滴加______________: | ①若无明显现象,证明固体中不含碳酸钠; ②若溶液变浑浊,证明固体中含有碳酸钠。 |
| 步骤3:向B试管中滴加______________: | 若溶液变浑浊,结合步骤2中的①,则假设 一成立:结合步骤2中的②,则假设二成立。 |
(4)己知C中有0.1 mol Cl2参加反应。若假设一成立,可推知C中反应的化学方程式为
。
(5)常温下Na2CO3和NaHCO3均为0.1mol/L的混合溶液中,c(OH﹣)-c(H+)=___________(用含碳元素的粒子浓度表示),在该溶液中滴加稀盐酸至中性时,溶液中溶质的成分有______________________。
查看答案和解析>>
科目: 来源: 题型:
SO2是一种重要的化工原料,也是一种环境污染物。
(1)SO2可用于工业制Br2过程中吸收潮湿空气中的Br2,反应的离子方程式是 。
(2)直接排放含SO2的烟气会形成酸雨,危害环境。用化学方程式表示SO2形成硫酸型酸
雨的反应: 。
(3)工业上用Na2SO3溶液吸收烟气中的SO2。
将烟气通入1.0 mol•L-1的Na2SO3溶液,溶液pH不断减小。当溶液pH约为6时,吸收SO2的能力显著下降,应更换吸收剂。
① 此时溶液中c(SO32-)的浓度是0.2 mol•L-1,则溶液中c(HSO3-)是_________mol•L-1,
由此说明NaHSO3溶液显 性,用化学平衡原理解释: 。
② 向pH约为6的吸收剂中通入足量的O2,可将其中的NaHSO3转化为两种物质,反应的化学方程式是 。
查看答案和解析>>
科目: 来源: 题型:
对羟基苯甲酸乙酯又称尼泊金乙酯,是一种常见的食品添加剂及防腐剂,其生产过程如下:(反应条件未全部注明)
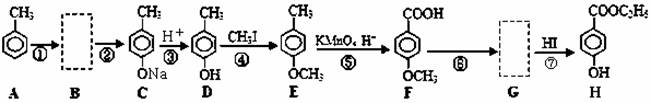
回答下列问题:
(1)D所含官能团的名称 。
(2)有机物G的结构简式 。
(3)反应④的反应类型是 。
(4)反应⑥的试剂和条件是 。
a.乙醇、浓H2SO4 b.乙酸、浓H2SO4 c.乙醇、稀H2SO4 d.乙酸、稀H2SO4
(5)下列四种物质不与H反应的是 。
a.FeCl3溶液 b.NaOH溶液 c.NaHCO3溶液 d.浓Br2水
(6)反应②的化学方程式是
(7)D有多种同分异构体,写出一个与D不同类且含苯环的结构简式: 。
查看答案和解析>>
科目: 来源: 题型:
化学反应原理在科研和生产中有广泛应用。
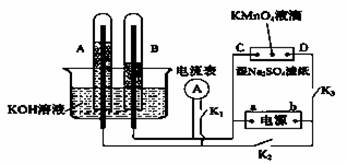 Ⅰ、如右图装置所示,A、B中的电极为多孔的惰性电极;C、D为夹在浸有Na2SO4溶液的滤纸条上的铂夹;电源有a、b两极。若A、B中充满KOH
Ⅰ、如右图装置所示,A、B中的电极为多孔的惰性电极;C、D为夹在浸有Na2SO4溶液的滤纸条上的铂夹;电源有a、b两极。若A、B中充满KOH
溶液后倒立于KOH溶液的水槽中。切断K1,闭合K2、K3通直流电。
回答下列问题:
(1) a是电源的 极,写出A中的电极反应式为_____。
(2)湿的Na2SO4滤纸条上能观察到的现象有____________。
(3)电解一段时间后,A、B中均有气体包围电极,若此时切断K2、K3,闭合K1,发现电流表的指针移动,写出此时B中的电极反应式为 。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
Ⅱ、甲醇是一种可再生能源,具有广泛的开发
和应用前景。工业上一般采用下列反应合成甲
 醇:CO(g)+2H2(g) CH3OH(g) ΔH,
醇:CO(g)+2H2(g) CH3OH(g) ΔH,
右表所列数据是该反应在不同温度下的化学平衡常数(K)。请回答下列问题:
(4)由表中数据判断ΔH 0(填“>”、“<”或“=”)。
(5)其他条件不变,只改变其中一个条件,下列措施可提高甲醇产率的是 。
A.升高温度 B.使用合适的催化剂 C.缩小容器的容积
D.充入过量的H2 E.恒压时,充入He F.从体系中分离出CH3OH
(6)某温度下,将2mol CO和6 mol H2充入2L密闭容器中,反应进行到4min末达到平衡,此时测得c(CO) =0.2 mol/L ,则0~4min内H2的反应速率为 ;若保持温度容积不变再向其中充入一定量的CH3OH,重新达到化学平衡状态,与原平衡状态相比,此时平衡混合气体中CH3OH的体积分数 (填“变大”、“变小”、或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
室温下,对于0.10 mol·L-1的氨水,下列判断正确的是( )
A.其溶液的pH=13
B.加入少量NaOH,溶液中c(NH4+)减小,Kw减小
C.与AlCl3溶液反应的离子方程式为 Al3++3OH―=Al(OH)3↓
D.滴加0.10 mol·L-1HNO3溶液到pH=7,溶液中离子浓度关系为:c (NO3―) = c(NH4+)> c(H+)=c(OH―)
查看答案和解析>>
科目: 来源: 题型:
t ℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)  2Z(g),各组分在不同时刻的浓度如下表:
2Z(g),各组分在不同时刻的浓度如下表:
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 2 min末浓度/mol·L-1 | 0.08 | a | b |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法正确的是
A.平衡时,X的转化率为20%
B.t ℃时,该反应的平衡常数为40
C.增大平衡后的体系压强, v正增大,v逆减小,平衡向正反应方向移动
D.前2 min内,用Y的变化量表示的平均反应速率v(Y) = 0.03 mol·L-1·min-1
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是
A.NaHCO3溶液中的水解:HCO3-+H2O H3O++CO32-
H3O++CO32-
B.氯化铁溶液中通入硫化氢:2Fe3++H2S=2Fe2++S↓+2H+
C.CaCl2 溶液中通入CO2: Ca2++CO2+H2O=CaCO3↓+2H+
D.NaHSO4溶液中逐滴加入Ba(OH)2溶液至恰好呈中性:
Ba2++OH-+H++SO42-=BaSO4↓+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com