
科目: 来源: 题型:
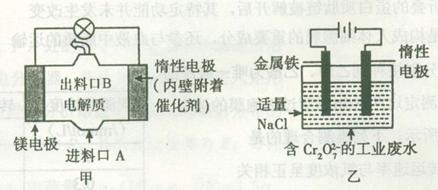
电化学在日常生活中用途广泛,图甲是镁一次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O==Cl-+Mg(OH)2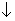 ,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
A.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2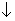
B.图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
C.图乙电解池中,若有0.084 g阳极材料参与反应,则阴极会有336 mL的气体产生
D.若图甲燃料电池消耗3.6 g镁产生的电量用以图乙废水处理,理论上可产生10.7 g氢氧化铁沉淀
查看答案和解析>>
科目: 来源: 题型:
25oC时,取浓度均为0.1 mol·L-1的醋酸溶液和氨水溶液各20 mL,分别用0.1 mol·L-1NaOH溶液、0.1 mol·L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示。下列说法正确的是
A.曲线I中滴加溶液到10 mL时: c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
B.曲线I中滴加溶液到25 mL时: c(NH4+)>c(C1-)>c(H+)>c(OH-)
C.曲线II中滴加溶液在10 mL~25 mL之间存在: c(NH4+)=c(Cl-)>c(OH-)=c(H+)
D.曲线II中滴加溶液到10mL时:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)]

查看答案和解析>>
科目: 来源: 题型:
CPAE是蜂胶的主要活性成分,由咖啡酸合成CPAE路线如下:
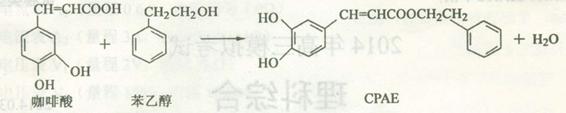
下列说法正确的是
A.苯乙醇属于芳香醇,它与邻甲基苯酚互为同系物
B.1 molCPAE最多可与含3 mol NaOH的溶液发生反应
C.用FeCl3溶液可以检测上述反应中是否有CPAE生成
D.咖啡酸、苯乙醇及CPAE都能发生取代、加成和消去反应
查看答案和解析>>
科目: 来源: 题型:
下列实验操作与预期实验目的或实验结论不一致的是
| 选项 | 实验操作及现象 | 实验目的或结论 |
| A | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 | 可证明氧化性:H2O2比Fe3+强 |
| B | 在0.1 mol·L-1的NaHCO3溶液中,加2滴酚酞显浅红色,微热,溶液颜色加深 | 验证盐类水解反应是吸热反应 |
| C | 将一定量的NaNO3和KCl的混合液加热并 浓缩至有晶体析出时,趁热过滤 | 得到NaCl晶体 |
| D | 苯酚钠溶液中通入足量二氧化碳产生浑浊 | 苯酚的酸性弱于碳酸 |
查看答案和解析>>
科目: 来源: 题型:
W、X、Y、Z是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或三种元素组成的化合物,己是由Y元素形成的单质,常温下丙和己均为气体。已知反应:甲+乙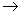 丁+己,甲+丙
丁+己,甲+丙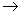 戊+己;常温下0.01 mol·L-1丁溶液的pH为12。下列说法正确的是
戊+己;常温下0.01 mol·L-1丁溶液的pH为12。下列说法正确的是
A.元素X在周期表中的位置为第2周期ⅥA族
B.元素X、Y、Z的原子半径由大到小的顺序为r(Z)>r(Y)>r(X)
C.1 mol甲与足量的乙完全反应转移的电子数为6.02×1023
D.1.0 L0.1 mol·L-1戊溶液中阴离子的总物质的量小于0.1 mol
查看答案和解析>>
科目: 来源: 题型:
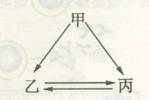
右图所示的甲、乙、丙三种物质均含有相同的某种元素,箭头表示物质间的转化一步就能实现,则甲可能是
①C ②H2O2 ③Na ④Fe ⑤HNO3
A.仅①③④ B.仅①②⑤
C.仅①②③⑤ D.①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
化学与生产生活、环境保护密切相关。下列说法中不正确的是
A.加热能杀死流感病毒是因为病毒的蛋白质受热变性
B.人造纤维、合成纤维和光导纤维都是有机高分子化合物
C.方便面的制作过程中常用到纯碱,葡萄酒中一般加入少量SO2作为添加剂
D.绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染
查看答案和解析>>
科目: 来源: 题型:
根据图示填空:

(1)化合物A中含有的官能团是 。
(2)1 mol A与2 mol H2反应生成1 mol E,其反应的化学方程式是 。
(3)与A具有相同官能团的A的同分异构体的结构简式是 。
(4)B经酸化后,与Br2反应得到D,D的结构简式是 。
(5)F的结构简式是 ,由E生成F的反应类型是 。
查看答案和解析>>
科目: 来源: 题型:
芳香化合物A是一种基本化工原料,可以从煤和石油中得到。A、B、C、D、E的转化关系如下所示:

回答下列问题:
(1)A的化学名称是 ;E属于 (填“饱和烃”或“不饱和烃”);
(2)A→B 的反应类型是 ,在该反应的副产物中,与B互为同分异构体的副产物的结构简式为 ;
(3)A→C的化学方程式为 ;
(4)A与酸性KMnO4溶液反应可得到D,写出D的结构简式 。
查看答案和解析>>
科目: 来源: 题型:
实验室制备1,2-二溴乙烷的反应原理如下:
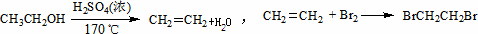
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚.
用少量溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据如右:

| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是 ;(填正确选项前的字母,下同)
a.引发反应 b.加快反应速度
c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置C中应加入 ,其目的是吸收反应中可能生成的酸性气体;
a.水 b.浓硫酸
c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的最简单方法是 ;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在 层(填“上”、“下”);
(5)若产物中有少量未反应的Br2,最好用 洗涤除去;
a.水 b.氢氧化钠溶液
c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚,可用 的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是 ;但又不能过度冷却(如用冰水),其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com