
科目: 来源: 题型:
用pH均为2的盐酸和醋酸溶液,分别中和等体积、等物质的量浓度的氢氧化钠溶液,当氢氧化钠恰好被完全中和时,消耗盐酸和醋酸溶液的体积分别为V1 和V2,则V1和V2的关系正确的是( )
A.V1>V2 B.V1<V2 C.V1=V2 D.V1≤V2
查看答案和解析>>
科目: 来源: 题型:
25℃时,水的电离达到平衡:H2O H++OH- DH>0,下列叙述正确的是( )
H++OH- DH>0,下列叙述正确的是( )
A. 向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B. 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C. 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D. 将水加热,KW增大,pH不变
查看答案和解析>>
科目: 来源: 题型:
用食用白醋(醋酸浓度约为1 mol/L)进行下列实验,能证明醋酸为弱电解质的是( )
A. 白醋中滴入石蕊试液呈红色 B. 白醋加入豆浆中有沉淀产生
C. 蛋壳浸泡在白醋中有气体放出 D. pH试纸显示醋酸的pH为2~3
查看答案和解析>>
科目: 来源: 题型:
用0.1026mol·L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,
滴定达终点时,滴定管中的液面如右图所示,正确的读数为( )
A. 22.30mL B. 22.35mL
C. 23.65mL D. 23.70 mL

查看答案和解析>>
科目: 来源: 题型:
下列离子方程式中,属于水解反应的是( )
A.CH3COOH + H2O  CH3COO- + H3O+ B.CO2 + H2O
CH3COO- + H3O+ B.CO2 + H2O  HCO3- + H+
HCO3- + H+
C.F- + H2O  HF + OH- D.HS-+ H2O
HF + OH- D.HS-+ H2O  S2- + H3O+
S2- + H3O+
查看答案和解析>>
科目: 来源: 题型:
[物质结构与性质]原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E元素原子序数为29。请用元素符号或化学式回答下列问题:
(1)X、Y、Z的第一电离能由小到大的顺序为 ▲ ;
(2)已知YZ与XQ2互为等电子体,则1 mol YZ中含有π键数目为____▲___;
(3)Z的气态氢化物沸点比Q的气态氢化物高的多,其原因是 ▲ ;
 (4)X、Z与氢元素可形成化合物H2X2Z4,常用作工业除锈剂。H2X2Z4分子中X的杂化方式为 ▲ ;
(4)X、Z与氢元素可形成化合物H2X2Z4,常用作工业除锈剂。H2X2Z4分子中X的杂化方式为 ▲ ;
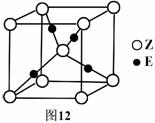
(5)E原子的核外电子排布式为 ▲ ;E有可变价态,它的某价态的离子与Z的阴离子形成晶体的晶胞如图12所示,该晶体的化学式为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s) + 3C(石墨) = 2Fe(s) + 3CO(g) △H 1 = +489.0 kJ·mol-1
C(石墨) +CO2(g) = 2CO(g) △H 2 = +172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 ▲ 。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K= ▲ 。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应。反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图10所示,则该反应的ΔH ▲ 0(填“>”、“<”或“=”)。

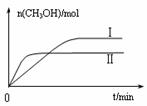
图10 图11
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图11所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ ▲ KⅡ(填“>”、“<”或“=”)。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为 ▲ 。当氨碳比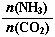 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为
▲ 。
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com