
科目: 来源: 题型:
下列试剂的保存方法不正确的是
A.NaOH溶液保存在配有玻璃塞的细口瓶中
B.金属钠通常密封保存在煤油中
C.氯水通常保存在棕色细口瓶并置于阴凉处
D.在盛液溴的试剂瓶中加水,形成“水封”,以减少溴挥发
查看答案和解析>>
科目: 来源: 题型:
下图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是
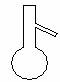

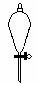
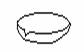
A.蒸馏、蒸发、分液、过滤 B.蒸馏、过滤、分液、蒸发
C.分液、过滤、蒸馏、蒸发 D.过滤、蒸发、分液、蒸馏
查看答案和解析>>
科目: 来源: 题型:
目前大量的照明材料或屏幕都使用了发光二极管(LED)。市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。试回答:
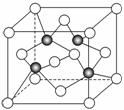
(1)镓的基态原子的价电子排布式是_______。砷原子的杂化轨道类型是 。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为________,与同一个镓原子相连的砷原子构成的空间构型为________。与砷原子紧邻的等距砷原子数为 。
(3)下列说法正确的是________。
A.砷化镓晶胞结构与NaCl相同 B.电负性:As>Ga
C. GaP与GaAs晶体类型相同,则前者熔点高 D.砷化镓晶体中含有配位键
(4)已知砷化镓的摩尔质量为M g/mol,该晶体的密度是ρ g/pm3 ,则砷原子半径为 ___________pm
查看答案和解析>>
科目: 来源: 题型:
(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有________(填序号,以下同),含有金属离子的物质是________,分子间可形成氢键的物质是________,属于离子晶体的是________,属于原子晶体的是________,①~⑤五种物质的熔点由高到低的顺序是__________________________。
(2)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500℃
试推断它们的晶体类型:A.________;B.________;C.________;D.________。
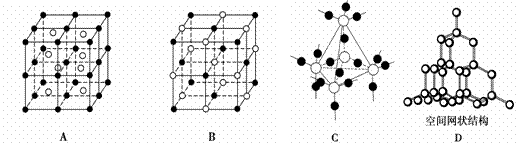
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:
A.____________;B._____________;C.___________;D.____________。

查看答案和解析>>
科目: 来源: 题型:
配位化合物因其特殊的结构与性质具有多方面的用途。
Ⅰ. 已知信息:[Ag(NH3)2] OH== [Ag(NH3)2]++OH—; [Ag(NH3)2]+ Ag++2NH3
Ag++2NH3
有两种化合物,A:COCl3·5NH3·H2O;B:COCl3·5NH3·H2O,根据下面的实验结果,确定它们的配离子、中心离子和配体。
⑴分别取A和B的固体于试管中微热,A中未见明显现象,B中试管口出现少量水珠。
⑵向A和B的溶液中加入AgNO3溶液后均有AgCl沉淀。
⑶沉淀过滤后,分别向滤液中加AgNO3溶液均无变化,但加热煮沸,B溶液中又有AgCl沉淀生成,其沉淀量为原来B溶液中AgCl的一半。
又已知该化合物中心离子配位数均为6,试按照“[Ag(NH3)2] OH”的书写格式写出A、B的化学式: A ___________________,B _____________________。
Ⅱ.Pt(NH3)2Cl2可以形成两种固体,一种为淡黄色,在水中的溶解度小,另一种为黄绿色,在水中的溶解度较大,请回答下列问题:
(1)Pt(NH3)2Cl2分子是 (填“平面四边形”或“四面体形”)
(2)请在以下空格内画出这两种固体分子的几何构型图:
 | |||
 |
淡黄色固体 黄绿色固体
(3)淡黄色固体物质是由 分子组成,黄绿色固体物质是由 分子组成(填“极性”或“非极性”)
(4)黄绿色固体在水中溶解度比淡黄色固体大,原因是 。
查看答案和解析>>
科目: 来源: 题型:
在新材料领域,碳族元素有许多应用,请用所学相关知识回答下列问题:
(1)碳纳米管由单层或多层石墨层卷曲而成,其结构类似于石墨晶体,每个碳原子通过________杂化与周围碳原子成键,多层碳纳米管的层与层之间靠__________结合在一起。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为____________。CH4的熔点比SiH4 (填“高”或“低”),原因是
。
(3)用价层电子对互斥理论推断SnBr2分子中Sn—Br键的键角______120°(填“>”、“<”或“=”),原因是___________________________________________.
(4)铅、钡、氧形成的某化合物的晶胞结构是:Pb4+处于立方晶胞顶点,Ba2+处于晶胞中心,O2-处于晶胞棱边中心。该化合物化学式为___________,每个Ba2+与_________个O2-配位。
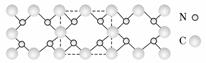
(5)氮化碳结构如下图,其中β氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料。在氮化碳晶体中每个碳原子与 个氮原子相连,每个氮原子与 个碳原子相连,化学式为___________。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为: ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2。回答下列问题:
(1)写出下列元素的符号:A _________ B__________ C __________
(2)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最小的元素是______,电负性最大的元素是_______。
(3)D的氢化物比C的氢化物的沸点______(填"高"或"低"),原因________________
(4)E元素原子的核电荷数是__________,E元素在周期表的位置是________________,已知元素周期表可按电子排布分为s区、p区等,则E元素在_______区。
(5)画出D的核外电子排布图___________________________________________,这样排布遵循了构造原理、_________原理和_________。]
查看答案和解析>>
科目: 来源: 题型:
据某科学杂志报道,国外一研究所发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60结构。下列叙述正确的是 ( )
A.该物质有很高的熔点、很大的硬度 B.该物质形成的晶体属分子晶体
C.该物质分子中Si60被包裹在C60里面 D.该物质的摩尔质量为1200 g/mol
查看答案和解析>>
科目: 来源: 题型:
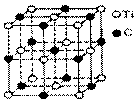
最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,分子模型如右图所示,其中圆圈表示钛原子,黑点表示碳原子,则它的化学式为( )
A.TiC B.Ti13C14 C.Ti4C7 D.Ti14C13
查看答案和解析>>
科目: 来源: 题型:
下图是氯化铵晶体的晶胞,已知晶体中2个最近的NH 核间距离为a cm,氯化铵的相对分子质量为M,NA为阿伏加德罗常数,则氯化铵晶体的密度(单位g·cm-3)为( )
核间距离为a cm,氯化铵的相对分子质量为M,NA为阿伏加德罗常数,则氯化铵晶体的密度(单位g·cm-3)为( )
 A.
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com