
科目: 来源: 题型:
下列关于甲烷的说法正确的是( )
A.甲烷分子中C、H间是非极性键
B.甲烷分子是空间三角锥结构
C.甲烷的结构式为CH4
D.甲烷分子中4个碳氢键是完全等同的
查看答案和解析>>
科目: 来源: 题型:
某兴趣小组研究SO2气体还原Fe3+、I2,他们使用的药品和装置如下图所示:
(1)SO2气体与Fe3+反应的主要产物是_____________、 。(填离子符号)
 (2)下列实验方案可以用于在实验室制取所
(2)下列实验方案可以用于在实验室制取所
需SO2的是 。
A.Na2SO3溶液与HNO3
B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.铜与热浓H2SO4
(3)装置C的作用是 。
(4)如果有280mL SO2气体(已折算为标态)
进入C装置中,则C中,50mL NaOH溶液
的浓度至少为 mol/L才能达到目的。
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A 中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去。
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第二份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的是 ,原因是 。
(6)能表明I—的还原性弱于SO2的现象是 ,
写出有关离子方程式:
查看答案和解析>>
科目: 来源: 题型:
在温度t ℃下,某Ba(OH)2的稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12, 向该溶液中逐滴加入pH=b的盐酸,测得混合溶液的部分pH如下表所示:
| 序号 | 氢氧化钡的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 8 |
| ② | 22.00 | 18.00 | 7 |
| ③ | 22.00 | 22.00 | 6 |
(1)依据题意判断,t ℃____25℃(填“大于”、“小于”或“等于”),该温度下水的离子积Kw=_____。
(2)b=____________,原Ba(OH)2的稀溶液的物质的量浓度为_____________。
(3)该温度下,向1L硫酸与硫酸钠的混合溶液中加入3L该Ba(OH)2的稀溶液时,沉淀正好达 最大量,从所得溶液中取出4mL并加水稀释至20mL,测得溶液的pH为7,则原硫酸与硫酸 钠混合溶液的pH为_________,以及其中Na2SO4的物质的量浓度为_________。
查看答案和解析>>
科目: 来源: 题型:
向一容积不变的密闭容器中充入一定量A和B,发生如下反应:
x A(g)+2B(s)  y C(g);△H <0在一定条件下,容器中 A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
y C(g);△H <0在一定条件下,容器中 A、C的物质的量浓度随时间变化的曲线如下图。请回答下列问题:
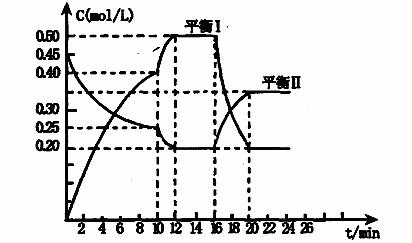
(1)用A的浓度变化表示该反应0~10min内的平均反应速率v(A)= ;
(2)根据图示可确定x:y= ;
(3)0~l0min容器内压强____ (填 “变大”,“不变”或“变小”)
(4)推测第l0min引起曲线变化的反应条件可能是 (填序号);第16min引起曲线变
化的反应条件可能是____ (填序号);
①减压;②增大A的浓度;③增大C的量;④升温;⑤降温;⑥加催化剂
(5)若平衡I的平衡常数为K1,平衡Ⅱ平衡常数为K2,则K1 K2(填“>”“=”或“<”)
查看答案和解析>>
科目: 来源: 题型:
工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
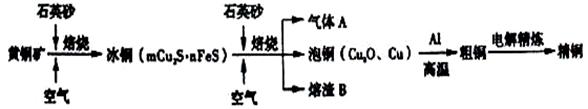
(1)气体A中的大气污染物可选用下列试剂中的 吸收。
A.浓H2SO4 B. 氨水 C.NaOH溶液 D.稀HNO3
(2)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,检验溶液中还存 在Fe2+的方法是 (注明试剂、现象)。
(3)由泡铜冶炼粗铜的化学反应方程式为 。
(4)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼, 下列说法正确的是 。
a.粗铜接电源正极,发生氧化反应 b.溶液中Cu2+向阳极移动
c.利用阳极泥可回收Ag、Pt、Au等金属 d.电能全部转化为化学能
(5)利用反应2Cu+H2O2+H2SO4==CuSO4+2H2O可制得CuSO4,若将该反应设计为原电池,其
正极电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
(1)图甲是实验室常用的一种仪器,其名称是____ ;其主要用途是________;
(2)小明用某规格的量筒量取一定体积的液体,液面位置如图乙,
则其量得液体体积为 (用a、b来表示)
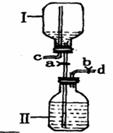
(3)右下图是某研究性小组设计的一个储气装置图。
①将气体存于Ⅱ瓶中,下列说法不正确的是 。
A.打开止水夹a,b,将气体从导管d通入,可将气体储存在Ⅱ瓶中
B.作为储气或取气时都无需在C处安装止水夹
C.该装置主要缺陷是C导管上未装止水夹
D.该装置也可用作制取氢气的发生装置;
②要从该储好气的装置中取用气体,正确操作是: 。

查看答案和解析>>
科目: 来源: 题型:
3.04g铜镁合金完全溶解于含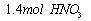 的浓HNO3中,得到NO2和N2O4混合气2240mL(标 准状况下)。向反应后的溶液中加入2mol
的浓HNO3中,得到NO2和N2O4混合气2240mL(标 准状况下)。向反应后的溶液中加入2mol L-1NaOH溶液,当金属离子全部沉淀时,得到5.08g 沉淀,下列说法不正确的是( )
L-1NaOH溶液,当金属离子全部沉淀时,得到5.08g 沉淀,下列说法不正确的是( )
①该合金中镁与铜的物质的量之比为1:2
②NO2和N2O4的混合气体中,N2O4的体积分数为80%
③得到5.08g沉淀时,加入NaOH溶液的体积是620mL
④该反应中共转移电子为1.2NA
A.③ B.②③④ C.①③ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
将1 mol A(g)和2 mol B(g)置于2L某密闭容器中,在一定温度下发生反应:
A(g)+B(g) C(g)+D(g),并达到平衡。C的体积分数随时间变化如下图I中曲线b所示,反 应过程中的能量变化如图II所示,下列说法不正确的是( )
C(g)+D(g),并达到平衡。C的体积分数随时间变化如下图I中曲线b所示,反 应过程中的能量变化如图II所示,下列说法不正确的是( )
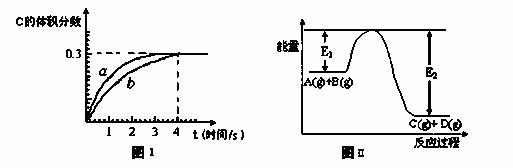
A.在上述反应体系中加入催化剂,化学反应速率增大,E1和E2均减小
B.该温度下,反应的平衡常数数值约为7.36
C.恒温条件下,缩小反应容器体积可以使反应 的过程按图I中a曲线进行
| |
查看答案和解析>>
科目: 来源: 题型:
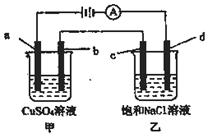
如图所示a、b、c均为石墨电极,d为碳钢电极,通电 进行电解。假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
A.甲、乙两烧杯中溶液的pH均保持不变
B.甲烧杯中a的电极反应式为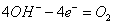 ↑+2H2O
↑+2H2O
C.当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀
D.当b极增重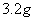 时,d极产生的气体为
时,d极产生的气体为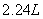 (标况)
(标况)
查看答案和解析>>
科目: 来源: 题型:
已知0.1mol·L-1的醋酸溶液中存在电离平衡:
CH3COOH CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)
的值增大,可以采取的措施是 ( )
①加少量烧碱溶液 ②升高温度 ③加少量冰醋酸 ④加水
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com