
科目: 来源: 题型:
2013年6月20日,中国首次太空授课活动成功举行,神舟十号航天员王亚平在天宫一号展示了失重环境下的物理现象。若在天宫一号中进行以下实验,其中最难完成的是( )
A.将金粉和铜粉混合 B.将牛奶加入水中混合
C.蒸发食盐水制取食盐晶体 D.用漏斗、滤纸过滤除去水中的泥沙
查看答案和解析>>
科目: 来源: 题型:
下列溶液配制实验的描述完全正确的是
A.在容量瓶中先加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸
B.用浓盐酸配制1:1(体积比)的稀盐酸(约6 mol.L-1)通常需要用容量瓶等仪器
C.配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4以防水解
D.用PH=1的盐酸配制100mL, PH=2的盐酸所需全部玻璃仪器有100mL容量瓶、烧杯、玻璃棒、胶头滴管
查看答案和解析>>
科目: 来源: 题型:
下列实验操作或实验结论正确的是
A.实验室用如图所示装置制取少量氨气

B.实验室制硝基苯时,将硝酸与苯混合后再滴加浓硫酸
C.实验室制溴苯时,将苯与液溴混合后加到有铁丝的反应容器中
D.醋酸钠结晶水合物与碱石灰共热制取甲烷
查看答案和解析>>
科目: 来源: 题型:
下列关于实验操作的叙述正确的是
A.酸碱滴定时,眼睛一定要注视滴定管中液面的变化
B.实验室制乙烯时,为使受热均匀,应轻轻搅动温度计
C.纸上层析实验中,须将滤纸上的试样点浸入展开剂中
D.分液时,下层液体先从分液漏斗下口放出,上层液体后从上口倒出
查看答案和解析>>
科目: 来源: 题型:
短周期元素A、B、C、D、E原子序数依次增大。A是周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C是自然界含量最多的元素,D是同周期中金属性最强的元素,E的负一价离子与C的某种氢化物W分子含有相同的电子数。
(1)A、C、D形成的化合物中含有的化学键类型为 ;W的电子式 。
(2)已知:①2E· → E-E;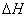 =-a kJ·mol-1 ② 2A· → A-A;
=-a kJ·mol-1 ② 2A· → A-A;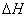 =-b kJ·mol-1 ③E·+A· → A-E;
=-b kJ·mol-1 ③E·+A· → A-E;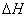 =-c kJ·mol-1
=-c kJ·mol-1
写出298K时,A2与E2反应的热化学方程式 。
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g) X(g);
X(g);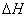 =-a KJ·mol-1(a>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
=-a KJ·mol-1(a>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 |
|
|
|
①在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则A2的平均反应速率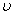 ( A2)为 。
( A2)为 。
②该温度下此反应的平衡常数K的值为 。
③下列现象能说明甲容器中的反应已经达到平衡状态的有 (填序号)。
A. 容器内A2、BC、X的物质的量之比为2:1:1
B. 容器内气体的密度保持恒定
C. 容器内A2气体的体积分数保持恒定
D.2V正(A2)=V逆(BC)
④三个容器中的反应分别达平衡时各组数据关系正确的是 (填序号)。
A.α1+α2=1 B.Q1+Q2=a C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0mol F.Q3=2Q1
(4)在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为75%,请在上图中画出第5min 到新平衡时X的物质的量浓度的变化曲线。
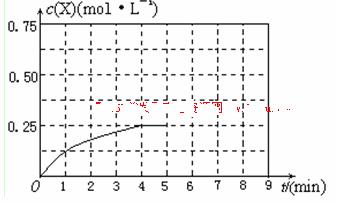
查看答案和解析>>
科目: 来源: 题型:
苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原理:
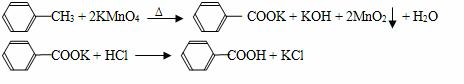
实验方法:一定量的甲苯和适量的KMnO4溶液在100℃反应一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的甲苯。
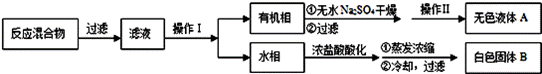
已知:苯甲酸相对分子质量122 ,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物一般都有固定熔点。
(1)操作Ⅰ为 ,需要用到的主要玻璃仪器为 ;
操作Ⅱ为 。
(2)无色液体A是 ,定性检验A的试剂是 ,
现象是 。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确.请在答题卡上完成表中内容。
| 序号 | 实验方案 | 实验现象 |
|
| ① | 将白色固体B加入水中, 加热溶解, | 得到白色晶体和无色溶液 | |
| ② | 取少量滤液于试管中,
| 生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体, |
| 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220 g产品溶解在甲醇中配成100 ml溶液,移取2 5.00 ml溶液,滴定,消耗KOH的物质的量为2.40 × 10 -3 mol,产品中苯甲酸质量分数的计算表达式为 ,计算结果为 。(保留两位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
某芳香烃A是一种重要的有机化工原料,以它为初始原料经过如下转化关系(部分产物、合成路线、反应条件略去)可以合成邻氨基苯甲酸、扁桃酸等物质。其中D能与银氨溶液发生银镜反应,H是一种功能高分子。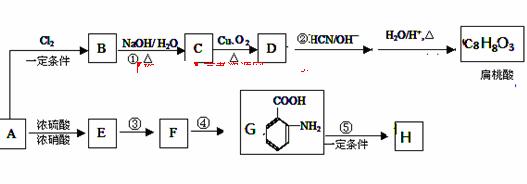
(1)写出扁桃酸的结构简式: ;写出G官能团的名称 。
(2)反应②的反应类型为: ;发生反应④的条件为加入 。
反应步骤③与④不能对换,其理由是 。
(3)写出D与银氨溶液反应的化学方程式: 。
(4)写出反应⑤的化学方程式: 。
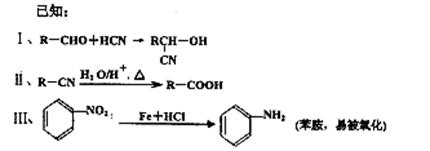
(5)写出符合下列条件G的同分异构体的结构简式 , ;(任写两种)
①含有苯环,且苯环上的一氯取代产物只有二种;
②苯环上只有两个取代基,且N原子直接与苯环相连 ;
③结构中不含醇羟基和酚羟基;
(6)请设计合理的方案以乙烯为主要有机原料合成。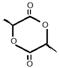
提示:①合成过程中无机试剂任选;② 合成路线流程图示例如下:
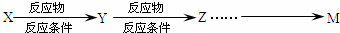


查看答案和解析>>
科目: 来源: 题型:
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是地壳中含量最高的金属,K是一种红棕色气体,过量G与J溶液反应生成M。
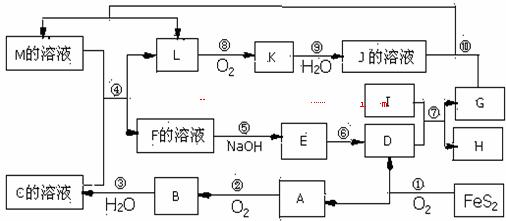
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第_______周期第_______族。
(2)在反应⑦中还原剂与氧化剂的物质的量之比为___________________。
(3)简述M溶液中阳离子的检验方法 。
(4)某同学取F的溶液,酸化后加入KI、淀粉溶液,变为蓝色。写出与上述变化过程相关的离子方程式: 。
(5)将化合物D与KNO3、KOH高温共熔,可制得一种“绿色”环保高效净水剂K2FeO4,同时还生成KNO2和H2O,该反应的化学方程式是_________________________。
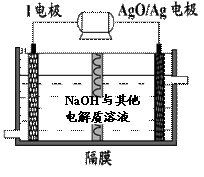 (6)镁与金属I的合金是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg与金属I的单质在一定温度下熔炼获得。
(6)镁与金属I的合金是一种潜在的贮氢材料,可在氩气保护下,将一定化学计量比的Mg与金属I的单质在一定温度下熔炼获得。
①熔炼制备该合金时通入氩气的目的是 。
② I电池性能优越,I-AgO电池可用作水下动力电源,其原理如图所示。该电池反应的化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池。下图为RFC工作原理示意图,有关说法正确的是:( )
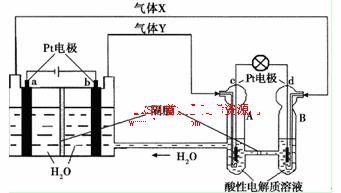
A.当有0.1 mol电子转移时,a极产生标准状况下1.12 L H2
B.左端装置中化学能转化为电能,右端装置中电能转化为化学能
C.c极上发生的电极反应是:O2 + 2H2O + 4e- = 4OH—
D.d极上进行还原反应,右端装置B中的H+可以通过隔膜进入A
查看答案和解析>>
科目: 来源: 题型:
常温下,用0.1000 mol·L-1 NaOH溶液分别滴定20.00 mL 0.1000 mol·L-1 盐酸和20.00 mL 0.1000 mol·L-1醋酸溶液,得到两条滴定曲线,如下图所示,若以HA表示酸,下列说法正确的是:( )
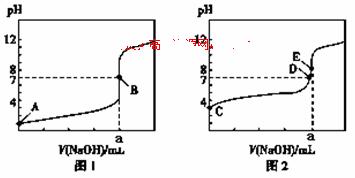
A.滴定盐酸的曲线是图2
B.达到B、E状态时,反应消耗的n(CH3COOH)>n(HCl)
C.达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A-)
D.当0 mL<V(NaOH)<20.00 mL时,对应混合液中各离子浓度大小顺序为
c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com