
科目: 来源:2014-2015江苏省泰州市姜堰区高一上学期期末化学试卷(解析版) 题型:填空题
(14分)结合氯气的相关知识解决下列问题。
(1)在实验室中制取Cl2,下列收集Cl2的正确装置是 (填字母)。
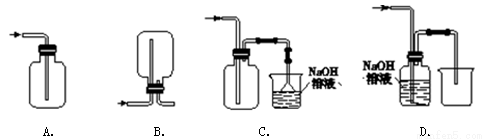
将Cl2通入水中,所得溶液中具有氧化性的含氯粒子有 。
(2)氯气可用于生产漂白粉。由于盐酸浓度不同,漂白粉与盐酸混合发生反应的反应类型不同。
漂白粉与稀盐酸发生复分解反应,离子方程式为 。
漂白粉与浓盐酸发生氧化还原反应,离子方程式为 。
(3)某实验小组向100mL FeI2溶液中逐渐通入Cl2,会依次发生如下反应:
a.Cl2+2I-=2Cl-+I2
b.Cl2+2Fe2+=2Cl-+2Fe3+
c.5Cl2+I2+6H2O=10Cl-+2IO3-+12H+
其中Fe3+、I2的物质的量随n(Cl2)的变化如图所示。
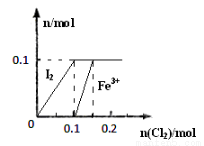
请回答下列问题:
①当n(Cl2)=0.12mol时,不考虑水的电离及金属离子的水解,分析溶液中所含金属阳离子及其
物质的量 (写出计算过程,否则不得分)。
②当溶液中n(Cl-):n(IO3-)=8:1时,通入的Cl2在标准状况下的体积为 L(写出计算过程,否则不得分)。
查看答案和解析>>
科目: 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列做法与可持续发展理念不符合的是
A.加大清洁能源的开发利用,提高资源的利用率
B.推广碳捕集和储存技术,逐步实现二氧化碳零排放
C.加大铅酸蓄电池、含汞锌锰干电池的生产,满足消费需求
D.对工业废水、生活污水净化处理,减少污染物的排放
查看答案和解析>>
科目: 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列化学用语书写正确的是
A.甲烷的电子式: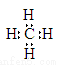
B.丙烯的键线式: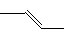
C.乙烯的结构简式:CH2CH2
D.乙醇的结构式: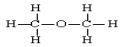
查看答案和解析>>
科目: 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
分子式为C7H16的烷烃中,含有3个甲基的同分异构体的数目是
A.2 B.3 C.4 D.5
查看答案和解析>>
科目: 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列物质的系统命名中,错误的是
A. 2,4-二甲基己烷
2,4-二甲基己烷
B.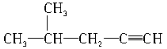 2-甲基-4-戊炔
2-甲基-4-戊炔
C.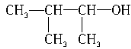 3-甲基-2-丁醇
3-甲基-2-丁醇
D.CH3—CHBr—CHBr—CH3 2,3-二溴丁烷
查看答案和解析>>
科目: 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
常温下,下列溶液中各组离子一定能大量共存的是
A.使甲基橙呈红色的溶液中:Na+、AlO2-、NO3-、CO32-
B.由水电离产生的c(H+)=10-12mol·L-1的溶液:NH4+、SO42-、HCO3-、Cl-
C.c(H+)/c(OH-)= 1×1014的溶液: Ca2+、Na+、ClO-、NO3-
D.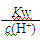 =0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3-
=0.1 mol·L-1的溶液:Na+、K+、CO32-、NO3-
查看答案和解析>>
科目: 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
设NA 为阿伏加德罗常数的值。下列说法正确的是
A.1 L 0.1mol·L-1的氨水含有0.1NA个OH-
B.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
C.在电解精炼粗铜的过程中,当阴极析出32 g铜时转移电子数为NA
D.25℃时,pH =13的Ba(OH)2溶液中含有OH-的数目为0 .1 NA
查看答案和解析>>
科目: 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.铅蓄电池放电时的负极和充电时的阳极均发生还原反应
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C.N2(g)+3H2(g) 2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大
2NH3(g) △H<0,其他条件不变时升高温度,反应速率v(H2)和氢气的平衡转化率均增大
D.纯碱溶于热水中去污效果增强,说明纯碱的水解是放热反应
查看答案和解析>>
科目: 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式正确的是
A.HCO3-的水解方程式为:HCO3-+H2O H2CO3+OH—
H2CO3+OH—
B.氢氧燃料电池的负极反应式:O2 + 2H2O + 4e-=4OH-
C.用铜做电极电解NaCl溶液:2Cl-+2H2O Cl2↑+H2↑+2OH—
Cl2↑+H2↑+2OH—
D.用惰性电极电解CuCl2溶液:2Cu2++2H2O 4H++O2↑+2Cu
4H++O2↑+2Cu
查看答案和解析>>
科目: 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。CO可用于炼铁,已知:Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH 1=+489.0 kJ·mol-1,
C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1 ;则CO还原Fe2O3(s)的热化学方程式为
A.Fe2O3+ 3CO=2Fe+ 3CO2 △H =-28.5 kJ·mol-1
B.Fe2O3(s)+ 3CO(g)=2Fe(s)+ 3CO2(g) △H =-28.5 kJ
C.Fe2O3(s)+ 3CO(g)=2Fe(s)+ 3CO2(g) △H = + 28.5 kJ·mol-1
D.Fe2O3(s)+ 3CO(g)=2Fe(s)+ 3CO2(g) △H =-28.5 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com