
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
25℃时,水的电离达到平衡:H2O H+ + OH-,下列叙述正确的是
H+ + OH-,下列叙述正确的是
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
查看答案和解析>>
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.草酸溶液与酸性KMnO4溶液混合后,由于生成物对反应有催化作用,会使反应速率加快
B.KI、H2SO4、淀粉溶液混合后,高温时出现蓝色时间反而较短,可能是因为高温时此反应较慢
C.恒温下,将盛有NO2和N2O4的平衡体系加压,体系颜色最终变浅
D.在K2Cr2O7溶液中滴加浓硫酸,溶液颜色由橙变黄(Cr2O72-为橙色)
查看答案和解析>>
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列各组离子中,在给定条件下能大量共存的是
A.在pH = 1的溶液中:NH4+、K+、ClO-、Cl-
B.有SiO32-存在的溶液中:Na+、Mg2+、Al3+、Cl-
C.有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+ 、Br-
D.在c(H+) = 1.0×10-13 mol·L-1的溶液中:Na+、S2-、AlO2-、SO32-
查看答案和解析>>
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g) + O3(g) N2O5(g) + O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
N2O5(g) + O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
A | B | C | D |
|
|
|
|
升高温度, 平衡常数减小 | 0~3 s内,反应速率为 v(NO2) = 0.2 mol·L-1 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
强酸溶液A与强碱溶液B,在常温下其pH之和为15,当它们按一定体积比混合时,溶液的pH恰好为7,则A与B的体积比为
A.1∶1 B.2∶1 C.1∶10 D.10∶1
查看答案和解析>>
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
某同学组装了如图所示的电化学装置,电极Ⅰ为 Zn,电极Ⅱ为Cu,其他电极均为石墨,则下列说法正确的是
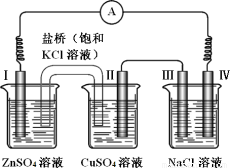
 A.电流方向:电极Ⅳ → ○ → 电极Ⅰ
A.电流方向:电极Ⅳ → ○ → 电极Ⅰ
B.盐桥中的K+会移向ZnSO4溶液
C.处得到标况下气体2.24L,电极II上析出6.4g固体
D.NaCl溶液中,电极Ⅲ制得氯气,电极Ⅳ制得金属钠
查看答案和解析>>
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.KSp[MgF2]>KSp[Mg(OH)2],不能实现Mg(OH)2转化为MgF2。
B.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大
C.等物质的量浓度的NH4Cl溶液和NH4HSO4溶液,后者的c(NH4+)大
D.FeCl3与KSCN反应达到平衡时,加入KCl溶液,则溶液颜色变深
查看答案和解析>>
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列各溶液中,微粒的物质的量浓度关系正确的是
A.0.1 mol/L Na2CO3溶液:c(OH-) = c(HCO3-) + c(H+) + 2c(H2CO3)
B.0.1 mol/L NH4Cl溶液:c(NH4+ ) = c(Cl-)
C.向醋酸钠溶液中加适量醋酸,得到的酸性混合溶液:c(Na+) > c(CH3COO-) > c(H+) > c(OH-)
D.向硝酸钠溶液中滴加稀盐酸得到pH = 5的混合溶液:c(Na+) = c(NO3-)
查看答案和解析>>
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列装置或操作能达到目的的是
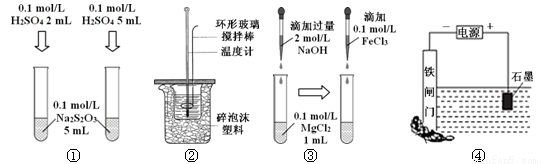
A.装置①探究H2SO4浓度对反应速率的影响
B.装置②可用于测定中和热
C.装置③探究Mg(OH)2能否转化成Fe(OH)3
D.装置④可保护铁闸门不被腐蚀
查看答案和解析>>
科目: 来源:2014-2015广东省广雅等四校高二上学期期末联考化学试卷(解析版) 题型:选择题
T℃时,向2.0 L恒容密闭容器中充入1.0 mol COCl2,反应COCl2(g) Cl2(g) + CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
Cl2(g) + CO(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t / s | 0 | 2 | 4 | 6 | 8 |
n(Cl2) / mol | 0 | 0.16 | 0.19 | 0. 20 | 0.20 |
下列说法正确的是
A.反应在前2 s 的平均速率v(CO) = 0.080 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(Cl2) = 0.11 mol·L-1,则反应的ΔH < 0
C.T℃时起始向容器中充入0.9 mol COCl2、0.20 mol Cl2和0.20 mol CO,达平衡前v正 > v逆
D.恒温恒容下,平衡后向体系内加入少量惰性气体,氯气的浓度不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com