
科目: 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:选择题
在下列各反应的离子方程式书写中,正确的是
A.将Na2O2放入水中发生的反应:Na2O2+2H2O=2Na++2OH-+O2↑
B.除去CuSO4溶液中的Fe3+:2 Fe3++3Cu=2Fe+3Cu2+
C.在KOH溶液中,甲烷-氧气燃料电池放电时的反应:CH4+2O2+2OH-=CO32-+ 3H2O
D.电解饱和食盐水制备H2和Cl2:2Cl-+2H+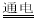 Cl2↑+H2↑
Cl2↑+H2↑
查看答案和解析>>
科目: 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:选择题
水的电离平衡曲线如图所示,下列说法中,正确的是
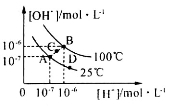
A.图中A、B、D三点处Kw的大小关系:B>A>D
B.25℃时,向pH=1的稀硫酸中逐滴加入pH=8的稀氨水,溶液中c(NH4+)/c(NH3·H2O)的值逐渐减小
C.在25℃时,保持温度不变,在水中加人适量NH4Cl固体,体系可从A点变化到C点
D.A点所对应的溶液中,可同时大量存在Na+、Fe3+、Cl-、SO42—
查看答案和解析>>
科目: 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:填空题
(17分)二氧化硫为重要的含硫化合物,是形成酸雨的主要污染物之一。
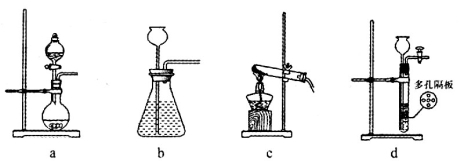
(1)在实验室中,若用70%的硫酸溶液和亚硫酸钠粉末反应制取二氧化硫,并要求方便控制反应速率,可选用下图所示气体发生装置中的_____(填下列序号字母)。
(2)SO2经催化氧化可生成SO3,该反应的热化学方程式为:2SO2(g)+O2(g) 2SO3(g) △H=a kJ·mol-1
2SO3(g) △H=a kJ·mol-1
在T1℃时,将2 mol SO2、1mol O2充入容积为2 L的密闭容器A中,充分反应并达到平衡,此过程中放出热量98.3 kJ,测得SO2的平衡转化率为50%,则a=_____,T1℃时,上述反应的平衡常数K1=____L·mol-1。若将初始温度为T1℃的2 mol SO2和1 molO2充入容积为2 L的绝热密闭容器B中,充分反应,在T2℃时达到平衡,在此温度时上述反应的平衡常数为K2。则K1______K2(填“>”、“<”或“=”)。
(3)某热电厂上空大气中所含二氧化硫严重超标,现对该区域雨水样品进行探究。首先用pH试纸测定雨水样品的pH,操作方法为___________________________,测得样品pH约为3;为进一步探究由SO3所形成酸雨的性质,将一定量的SO2通入蒸馏水中,配成pH为3的溶液,然后将溶液分为A、B两份,向A中加入适量的NaOH固体,使溶液恰好呈中性(不考虑氧化性物质和其它酸性物质的影响),则此中性溶液中离子的浓度间存在的关系式为:[Na+]=______________;将溶液B久置于空气中,与久置前相比,久置后的溶液B中水的电离程度将__________(填“增大”、“减小”或“不变”)。
(4)工业上常用如下图所示的流程处理工业尾气中的SO2:
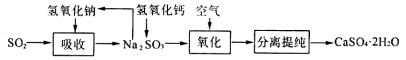
上述流程中有一种物质可以再生循环利用,该物质再生的化学方程式为___________________.
查看答案和解析>>
科目: 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:填空题
(16分)钢厂酸洗废液(成分如下表所示)在工业生产中还具有很多用途。

(1)欲检验该酸洗废液中含有的少量Fe3+,最宜选用的试剂是_____溶液;为检验其中的Fe2+,某同学设计了如下实验:取该酸洗废液少许加入试管中,滴入几滴酸性KMnO4溶液后发现紫色消失。该同学得出结论:该溶液中含有Fe2+。大家认为该同学的实验设计不合理,理由是____________________________(用必要的文字和离子方程式解释)。
(2)采用石墨作电极电解上述酸洗废液时,初始阶段,阳极板上有气泡生成,此时与该现象有关的阳极电极反应式为______;向上述酸洗废液中加入KOH溶液中和后,在合适的电压下电解,可在__________(填“阴”或“阳”)极生成高铁酸钾(K2FeO4)。
(3)利用上述酸洗废液、含铝矿石(主要成分为Al2O3、Fe2O3和SiO2)以及新制的硅酸(活化硅酸),制备聚硅酸氯化铝铁絮凝剂(简称PAFSC),具体方法如下:
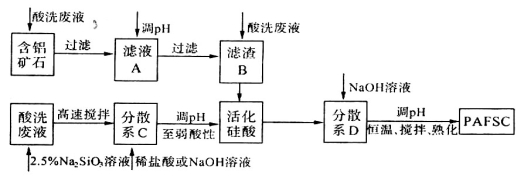
①适当调高滤液A的pH,Al3+和Fe2+转化为沉淀,原因是______________(请用沉淀溶解平衡的理论解释)。
②PAFSC絮凝剂净化水的过程中,Al3+参与反应的离子方程式为________________。
③25℃时,PAFSC的除浊效果随溶液pH的变化如图所示(图中的NTU为浊度单位),则在下列pH范围中,PAFSC除浊效果最佳的是______(填下列序号字母)。
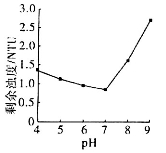
a.4~5 b.5~7 c.7~8 d.8~9
25℃时,pH>7且随pH增大,PAFSC的除浊效果明显变差,原因是碱性增强,使胶体发生了_____现象。
查看答案和解析>>
科目: 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:实验题
(20分)某小组的同学欲探究NH3经一系列反应得到HNO3和NH4NO3的过程,NH3的转化过程如下图所示。

甲、乙两同学分别按下图所示装置进行实验。
用于A、B装置中的可选药品:浓氨水、30%H2O2溶液、蒸馏水、NaOH固体、MnO2
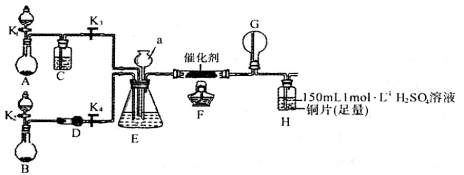
(1)仪器a的名称是____,装置A的圆底烧瓶中发生反应的化学方程式为___________________。装置E有多种作用,下列关于装置E的作用或其中所盛液体的说法中,不正确的是_________(填下列序号字母)。
a.使氨气和氧气充分混合 b.控制通入氨气和氧气的体积比
c.平衡装置内的压强 d.锥形瓶内液体是饱和食盐水
(2)甲同学先点燃酒精灯,再打开K1、K2、K3、K4,反应一段时间后,他认为成功模拟了过程Ⅱ的反应,原因是其观察到__________(填支持其观点的实验现象);甲同学进行的实验中产生的气体持续通入装置H一段时间后,H中的溶液变成蓝色,则其中铜片所参与反应的离子方程式为_____________,若制得的氨气仅按I→Ⅱ→III的顺序完全转化为硝酸,欲使H装置中所得溶液为纯净的CuSO4溶液(忽略Cu2+的水解),理论上所需氨气在标准状况下的体积为______L(假设硝酸与铜反应产生的还原产物全部排出反应装置);从所得CuSO4溶液中得到CuSO4·5H2O晶体的法是将溶液____、____、过滤、洗涤、干燥。
(3)乙同学为模拟过程IV的反应,在甲同学操作的基础上对该装置进行了下列各项中的一项操作,使G处圆底烧瓶中产生大量白烟,你认为这项操作是_____(填下列序号字母)。
a.关闭K3并熄灭酒精灯
b.关闭K4并熄灭酒精灯
c.关闭K3、K4并熄灭酒精灯
(4)丙同学认为该系列实验装置存在一处明显的设计缺陷,你认为该设计缺陷是______________。
查看答案和解析>>
科目: 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:填空题
(12分)【化学——化学与技术】黄铜矿在我国储量丰富,主要产地集中在长江中下游地区、川滇地区、山西南部中条山地区、甘肃的河西走廊以及西藏高原等。这种铜矿石所含主要成分为CuFeS2,某企业以其为原料炼制精铜的工艺流程示意图如下:
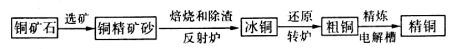
请回答下列问题:
(1)在反射炉中,把铜精矿砂和石英砂混合加热到l000℃,矿砂与空气反应生成冰铜(由Cu2S和FeS互相熔合而成)和大气污染物A,该过程中发生主要反应的化学方程式为_________________;A可用于海水提溴,在粗溴提纯环节中,A参与反应的化学方程式为__________________;利用反射炉中产生的矿渣可生产一种良好的无机高分子絮凝剂——聚硅酸铁,其具有净水作用。将下列各项中物质加入水中后,不具有类似聚硅酸铁的净水作用的是_____________(填下列序号字母)
a.明矾 b.硫酸镁 c.硫酸铁 d.硫酸铝
(2)冰铜所含铜元素的质量分数为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200℃左右吹入空气进行吹炼。冰铜中的部分Cu2S被氧化成Cu2O,生成的Cu2O再与Cu2S反应,得到粗铜,用一个反应的化学方程式表示利用冰铜生产粗铜的过程________,利用这种工艺生产2 t含铜量为98%的粗铜,至少需要铜元素含量为40%的冰铜_______t。
(3)以CuSO4溶液为电解液,电解精炼铜(粗铜中含Fe、Ag、Pt、Au等杂质)。下列说法中,正确的是______(填下列序号字母)。
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.电解液中Cu2+向阳极移动
d.从阳极泥中可回收Ag、Pt、Au等金属
查看答案和解析>>
科目: 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:填空题
(12分)【化学——物质结构与性质】硼在半导体工业中被大量用作半导体掺杂物,同时含硼化合物在杀虫剂、防腐剂及新型储氢材料的制造中也有重要的地位。请回答下列问题:
(1)在第2周期的元素中,基态原子的第一电离能小于硼的元素有_________种。
(2)硼砂是人们最早使用的含硼化合物之一,其阴离子Xm-( Xm-中只含B、O、H三种元素)的球棍模型如图所示,则在Xm-中,硼原子轨道的杂化类型分别为_____、_____;图中标注为2号的原子与相邻原子成键形成的键角_____4号原子与相邻原子成键形成的键角(填“大于”“小于”或“等于”)。在下列各项中,在Xm-内不存在的化学键是____(填下列序号字母)。
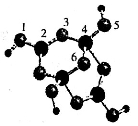
a.离子键 b.共价键 c.配位键
(3)氨硼烷(NH3BH3)与镧镍合金(LaNix)都是优良的储氢材料。镧镍合金的晶胞结构示意图如图所示(只有1个原子位于晶胞内部),则x=____。氨硼烷在高温下释放氢后生成的立方氮化硼晶体,具有类似金刚石的结构,硬度略小于金刚石。则在下列各项中,立方氮化硼晶体不可用作______(填下列序号字母)。
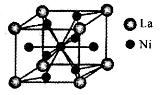
a.耐磨材料 b.切削工具 c.导电材料 d.钻探钻头
查看答案和解析>>
科目: 来源:2014-2015学年山东省济南市高三下学期一模考试理综化学试卷(解析版) 题型:填空题
(12分)【化学——有机化学基础】松油醇(G)可用于配制香精,其合成路线如下:
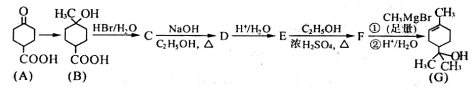
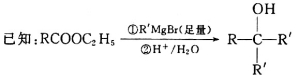
请回答下列问题:
(1)G所含两种官能团的名称分别是________、__________。
(2)同时符合下列两个条件的B的同分异构体有____________种。
i.含有六元碳环,碳环上仅有两个取代基且呈对位;
ii.在一定条件下能发生银镜反应、水解反应和消去反应。
(3)为了鉴别E和F,宜选用下列试剂中的_______作鉴别试剂(填下列序号字母)。
a.溴水 b.银氨溶液 c.酸性KMnO4溶液 d.NaHCO3溶液
(4)C→D的化学方程式为_________________。
(5)物质A(分子式为C7H10O3)催化氢化得到H(分子式为C7H12O3),H在一定条件下可以生成高聚物I,I的结构简式为_____________。
查看答案和解析>>
科目: 来源:2014-2015学年山东省济宁市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
运用化学知识判断,下列说法正确的是
A.地沟油的主要成分是高级脂肪酸甘油酯,可食用
B.NOx、SO2、CO2、PM2.5颗粒都会导致酸雨
C.高空臭氧层吸收太阳紫外线,保护地球生物;低空过量臭氧是污染气体,对人体有害
D.石油化工中的分馏、裂化、裂解都是通过化学反应来获得轻质油、气态烯烃
查看答案和解析>>
科目: 来源:2014-2015学年山东省济宁市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.标况下,1.12LCl2溶于水,转移0.05NA电子
B.向NH4Al(SO4)2稀溶液中逐滴加入过量Ba(OH)2溶液,离子方程式为:NH4++Al3++2SO42-+Ba2++5OH-=2BaSO4↓+AlO2-+2H2O+NH3·H2O
C.常温下,由水电离出的H+浓度为10-13mol·L-1的溶液中,Fe2+、Cl-、:Na+、NO3-可能大量共存
D.葡萄糖(C6H12O6)溶液中:SO42-、MnO42-、K+、H+可以大量共存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com