
科目: 来源: 题型:
在密闭容器中进行反应:2A+3B 2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是
2C。开始时C的浓度为amol·L-1,2min后C的浓度变为2amol·L-1,A和B的物质的量浓度均变为原来的1/2,则下列说法中不正确的是
A.用B表示的反应速率是0.75a mol/(L·min)
B.反应开始时,c(B)=3amol·L-1
C.反应2min后,c(A)=0.5amol·L-1
D.反应2min后,c(B)=1.5amol·L-1
查看答案和解析>>
科目: 来源: 题型:
同周期主族元素,随原子序数递增,下列说法中错误的是
A.最外层电子数逐渐增多 B.元素最高正化合价均由+1递增到+7
C.原子半径逐渐减小 D.金属性逐渐减弱,非金属性逐渐增强
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,错误的是
A.H2S、H2O、HF的稳定性依次增强
B.RbOH、KOH、Mg(OH)2的碱性依次减弱
C.Ca、Mg、Na的还原性依次减弱
D.H2SiO3、H2CO3、H2SO4的酸性依次增强
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.“钡餐”中使用的硫酸钡是弱电解质
B.太阳能电池板中的硅在周期表中处于金属与非金属的交界位置
C.常用的自来水消毒剂有Cl2和二氧化氯,两者都含极性键
D.“滴水穿石”不涉及化学变化
查看答案和解析>>
科目: 来源: 题型:
氨在国民经济中占有重要地位。
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
工业合成氨的热化学方程式是 。
(2)工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+ CO2 (g)  CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
| T / ℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
①ΔH(填“>”、“<”或“=”) 0。
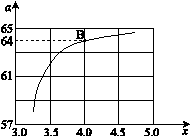
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)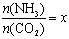 ,右图是氨碳比(x)与CO2平衡转化率(α%)的关系。α随着x增大而增大的原因是 。
,右图是氨碳比(x)与CO2平衡转化率(α%)的关系。α随着x增大而增大的原因是 。
③ 上图中的B点处,NH3的平衡转化率为 。
查看答案和解析>>
科目: 来源: 题型:
用实验确定某酸HA是弱电解质。两同学的方案如下:
甲:①称取一定质量的HA配制0.1 mol·L-1的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度和质量相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是________________。
(2)甲方案中说明HA是弱电解质的理由是测得溶液的pH______1
(选填“>”、“<”或“=”)。
(3)乙方案中说明HA是弱电解质的现象是 ____。
①装HCl溶液的试管中放出H2的速率快;
②装HA溶液的试管中放出H2的速率快;
③两个试管中产生气体的速率一样快。
(4)请你评价:乙方案中难以实现之处和不妥之处:
________________________________________________________________________。
(5)请你提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述:
_______________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com