
科目: 来源: 题型:
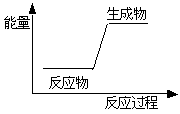
下列反应前后物质的总能量变化可用右图表示的是( )
A.生石灰加水生成熟石灰 B.C+H2O=CO+H2
C.金属钠与水反应 D.HNO3+NaOH=NaNO3+H2O
 |
查看答案和解析>>
科目: 来源: 题型:
对于100mL1mol/L盐酸与铁片的反应,采取下列措施:①升高温度;②改用100mL3mol/L盐酸;③多用300mL1mol/L盐酸;④用等量铁粉代替铁片;⑤改用98%的硫酸。其中能使反应速率加快的是( )
A.①③④ B.①②④ C.①②③④ D.①②③⑤
查看答案和解析>>
科目: 来源: 题型:
运用元素周期律分析下面的推断,其中错误的是( )
A.砹(85号元素)是一种有色固体,HAt应该不稳定,且AgAt是有色难溶于水固体
B.铍(Be)是一种金属,它的氧化物的水化物可能具有两性
C.硫酸锶(SrSO4)是难溶于水和盐酸的白色固体
D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体
查看答案和解析>>
科目: 来源: 题型:
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
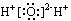 A.H2O的电子式: B.质量数为14的碳原子:
A.H2O的电子式: B.质量数为14的碳原子: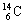
C.CO2的比例模型: D.Cl-的结构示意图:
D.Cl-的结构示意图:
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.在多电子的原子里,能量高的电子通常在离核近的区域内运动
B.最外层电子数为8的微粒均是稀有气体元素的原子
C.俄国化学家道尔顿为元素周期表的建立作出了巨大贡献
D.在周期表中金属和非金属的分界线附近寻找制备半导体材料
查看答案和解析>>
科目: 来源: 题型:
早期制硫酸的工艺流程中,涉及到反应:NO2 + SO2 = NO + SO3,该反应中SO2作( )
A. 氧化剂 B. 还原剂 C. 催化剂 D. 漂白剂
查看答案和解析>>
科目: 来源: 题型:
A~G是前四周期除稀有气体之外原子序数依次增大的七种元素。A与其它元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。请结合题目回答以下问题:
(1)元素名称:B ,G 。
(2)F的价电子排布图 。
(3)写出化合物BC的结构式 。
(4)离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是 。
 |
(6)B、C之间的元素K可以与A形成KA3,G的离子与KA3可形成[G(KA3)4]2+离子,1mol[G(KA3)4]2+离子中含有的σ键的物质的量为 mol。
(7)在测定A、D形成的分子的相对分子质量时,实验测定值一般高于理论值的主要原因是 。
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
| T | 常温常压下,T单质是淡黄色固体,常在火山口附近沉积 |
| P | P的价层电子排布为[Ar]3d104s2 |
(1)W位于元素周期表第________周期第________族;W的原子半径比X的________(填“大”或“小”)。
(2)TY2中心原子的杂化方式为_______;XY2中一个分子周围有__________个紧邻分子;堆积方式与XY2晶胞类型相同的金属有_________(从“Cu、 Mg、K、Po”中选出正确的),其空间利用率为_______。
(3)Z的第一电离能比Mg的________(填“大”或“小”);写出Z单质与NaOH溶液反应的化学方程式 。
(4)写出W的最高价氧化物与NaOH溶液反应的离子方程式 ;W的最高价氧化物与XY2的熔点较高的是 ,原因是 。
(5)处理含XO、TO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质T。已知:
XO(g)+ 1/2O2(g)====XO2(g) ΔH=-283.0 kJ·mol-1
T(s)+O2(g)=====TO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是______________________________。
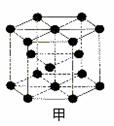
(6)P在周期表的 区;P和T形成的化合物PT在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方PT晶体结构如下图所示,其晶胞边长为540.0 pm,密度为_________ g·cm-3(列式并计算)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com