
科目: 来源: 题型:
实 验室中,用如下图所示装置及所给药品(图中部分夹持仪器已略去)探究工业制硫酸接触室中的反应,并测定此条件下二氧化硫的转化率。已知:SO3熔点为
验室中,用如下图所示装置及所给药品(图中部分夹持仪器已略去)探究工业制硫酸接触室中的反应,并测定此条件下二氧化硫的转化率。已知:SO3熔点为
16.8℃,假设气体进入装置时分别被完全吸收,且忽略装置内空气中的CO2。
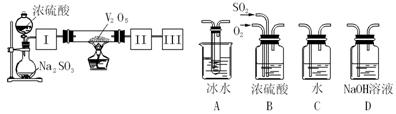
(1)已知0.5molSO2被O2氧化成气态SO3,放出49.15 kJ热量,此反应的热化学方程式为 ;
(2)根据实验目的,请从上面右图中选择Ⅰ、Ⅱ、Ⅲ处合适的装置,并将其字母填入空格中:装置Ⅰ ,装置Ⅱ ;
(3)开始进行实验时,首先应进行的操作是 ;
(4)停止通入SO2,熄灭酒精灯后,为使残留在装置中的SO2、SO3尽可能被充分吸收,操作方法是 ;
(5)实验结束后,若装置Ⅱ增加的质量为b g ,装置Ⅲ增加的质量为a g,则此条件下二氧化硫的转化率是: ×100%(用含字母的最简代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分。
| 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ | |||
| 四 | ⑾ | ⑿ | ⒀ |
(1)元素 的单质室温下呈液态;元素 的氢化物最稳定;元素 的最高价氧化物的水化物的酸性最强;元素 的高价氧化物的水化物的碱性最强(填写“元素符号”);
(2)表中元素③与⑨形成稳定化合物的结构式是 ;
(3)表中元素①③⑤组成的“A4B2C2”型物质,分子内含有的键型是 ;
A.离子键和共价键 B.仅为共价键
C.仅为极性共价键 D.极性共价键和非极性共价键
(4)表中元素 的氢化物的分子间存在氢键(填写“数字序号”);
查看答案和解析>>
科目: 来源: 题型:
如图是无机物A-M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体.D的俗名叫铁红,A是形成酸雨的主要气体。则:
(1)在周期表中,组成单质I的元素位于第 周期 族;
(2)写出S2-的离子结构示意图: ;写出N2的结构式: ;
(3)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应是 ;(填写序号)
(4)反应④的离子方程式是: 。

查看答案和解析>>
科目: 来源: 题型:
在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出 a kJ的热量。
(1) 写出肼和过氧化氢的电子式:肼: ,过氧化氢: ;
(2) 写出该反应的热化学方程式: ;
(3) 已知H2O(1)==H2O(g) △H= + b kJ/mol,则16g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是________________ kJ。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D是元素周期表中前三周期里的四种元素,A能与D组成AD2型化合物,AD2中核外电子总数是30。离子D-的核外电子排布与Al3+相同,B和C可以形成BC型化合物,BC分子中质子总数是18,BC水溶液是一种强酸,试回答:
(1) 用电子式表示BC的形成过程:___________________________________;
(2) D单质与水反应的化学方程式是:__________________________________;
(3) 比较AD2中两种微粒的半径:r(A2+)_________r(D-)(填“>”、“<”或“=”)
查看答案和解析>>
科目: 来源: 题型:
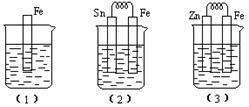
如下图所示,烧杯中都盛有稀硫酸:
① 装置(2)中Fe电极的电极反应:
,
装置(3)中Fe电极的电极反应:
;
② 装置(2)Sn极附近溶液的pH ;(填:“增大”、“减小”或“不变”)
③ 比较(1)、(2)、(3)中铁被腐蚀的速率由快到慢的顺序是 。(填“序号”)
查看答案和解析>>
科目: 来源: 题型:
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液体积是
A.60 mL B.45 mL C.30 mL D.15 mL
查看答案和解析>>
科目: 来源: 题型:
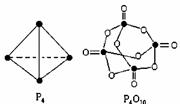
白磷与氧可发生如下反应:P4+5O2=== P4O10。已知断裂下列化学键需要吸收的能量分别为:P-P:a kJ·mol-1、P-O:b kJ·mol-1、P=O:c kJ·mol-1、O=O:d kJ·mol-1,根据图示的分子结构和有关数据估算该反应的 H,其中正确的是
H,其中正确的是
A. (6a+5d-4c-12b) kJ·mol-1
B. (4c+12b-6a-5d) kJ·mol-1
C. (4c+12b-4a-5d) kJ·mol-1
D. (4a+5d-4c-12b) kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
A+、B2+、C-、D2-四种离子具有相同电子层结构。现有以下排列顺序:
①B2+>A+>C->D2-;②C->D2->A+>B2+;③B2+>A+>D2->C-;④D2->C->A+>B2+ 。四种离子的半径由大到小以及四种元素原子序数由大到小的顺序分别是
A.①④ B.④① C.②③ D.③②
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、W有右图所示的转化关系,已知焓变:
ΔH=ΔH1+ΔH2,则X、Y可能是
①C、CO ②Na2CO3、NaHCO3 ③AlCl3、Al(OH)3 ④FeBr2、FeBr3
A.①②③④ B.①③ C.②④ D.①②③

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com