
科目: 来源: 题型:
能源的开发和利用是当前科学研究的重要课题。
(1)利用二氧化铈(CeO2)在太阳能作用下前实现如下变废为宝的过程:
mCeO2 (m-x)CeO2
(m-x)CeO2 xCe+xO2
xCe+xO2
(m-x)CeO2 xCe+xH2O+xCO2
xCe+xH2O+xCO2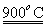 mCeO2+xH2+xCO
mCeO2+xH2+xCO
上述过程的总反应是 ,该反应将太阳能转化为 。
(2)CO、O2和KOH溶液构成的燃料电池的负极电极反应式为 。该电池反应可获得K2CO3溶液,某温度下0.5mol L-1。晦K2CO3溶液的pH=12,若忽略CO32-的第二级水解,则CO32- +H2O
L-1。晦K2CO3溶液的pH=12,若忽略CO32-的第二级水解,则CO32- +H2O HCO3-+OH-的平衡常熟Kh= 。
HCO3-+OH-的平衡常熟Kh= 。
(3)氯碱工业是高耗能产业,下列将电解池与燃料电池相组合的工艺可以节能30%以上。

①电解过程中发生反应的离子方程式是 ,阴极附近溶液PH (填“不变”、“升高”或“下降”)。
②如果粗盐中SO42-含量较高,精制过程需添加钡试剂除去SO42-,该钡试剂可选用下列试剂中的 。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
现代工艺中更多使用BaCO3除SO42-,请写出发生反应的离子方程式 。
③图中氢氧化钠溶液的质量分数a% b%(填“>”、‘‘=”或“<”),,燃料电池中负极上发生的电极反应为 。
查看答案和解析>>
科目: 来源: 题型:
合成氨技术的发明使工业化人工固氮成为现实。
(1)已知N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H=-92.2kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6LNH3时,放出的热量为 。
H=-92.2kJ·mol-1。在一定条件下反应时,当生成标准状况下33.6LNH3时,放出的热量为 。
(2)合成氨混合体系在平衡状态时NH3的百分含量与温度的关系如下图所示。由图可知:
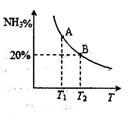 ①温度T1、T2时的平衡常数分别为K1、K2,则K1 K2 (填“>”或“<”)。若在恒温、恒压条件下,向平衡体系中通入氦气,平衡 移动、(填“向左”、“向右”或“不”)。
①温度T1、T2时的平衡常数分别为K1、K2,则K1 K2 (填“>”或“<”)。若在恒温、恒压条件下,向平衡体系中通入氦气,平衡 移动、(填“向左”、“向右”或“不”)。
②T2温度时,在1L的密闭容器中加入2.1mol N2、l.5molH2,经10min达到平衡,则v(H2)= 。达到平衡后,如果再向该容器内通入N2、H2、NH3各0.4mol,则平衡 移动(填“向左”、“向右”或“不”)。
(3)工业上用CO2和NH3反应生成尿素:CO2(g)+2NH3(g) H2O(1)+CO(NH2)2(1) △H,
H2O(1)+CO(NH2)2(1) △H,
在一定压强下测得如下数据:

①则该反应△H 0,表中数据a d,b f(均选填“>”、‘‘=”或“<”)。
②从尿素合成塔内出来的气体中仍含有一定量的CO2、NH3,应如何处理 。
查看答案和解析>>
科目: 来源: 题型:
 25℃时,满足c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的醋酸和醋酸钠混合溶液中,c(CH3COO-)与pH的关系如图所示。下列叙述错误的是
25℃时,满足c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的醋酸和醋酸钠混合溶液中,c(CH3COO-)与pH的关系如图所示。下列叙述错误的是
A.该温度下醋酸的电离常数Ka为l0-4.75mol·L-l
B.M点所表示的溶液中:
c(Na+)+c(H+)+c(CH3COOH)=0.1 mol·L-1
C.N点所表示的溶液中:
c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
D.Q点所表示的溶液中加入等体积的0.05mol·L-1NaOH溶液充分反应后pH>7
查看答案和解析>>
科目: 来源: 题型:
储氢合金表面镀铜过程发生反应Cu2++2HCHO+4OH-=Cu +H2
+H2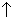 +2H2O+2HCOO-,下列说法错误的是
+2H2O+2HCOO-,下列说法错误的是
A.电镀过程中氢气在镀件表面析出
B.电镀时溶液中Cu2+移向阴极,并在阴极上发生还原反应
C.阳极反应式为HCHO+3OH--2e-=2H2O+HCOO-
D.电镀时每生成6.4g铜镀层放出2.24L H2
查看答案和解析>>
科目: 来源: 题型:
利用实验器材(规格和数量不限)能完成相应实验的一项是
| 选项 | 实验器材(省略夹持装置) | 相应实验 l |
| A | 三脚架、泥三角、坩埚、坩埚钳 | 用CuSO4 |
| B | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用浓盐酸配制0.1mol·L-1的HCl溶液 |
| C | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
| D | 烧杯、酸式滴定管、碱式滴定管 | 用H2SO4标准液滴定未知浓度的NaOH溶液 |
查看答案和解析>>
科目: 来源: 题型:
NA表示阿伏伽德罗常数的值,下列叙述错误的是
A.2gD216O中含有的质子数、中子数、电子数均为NA
B.80g CuO和Cu2S的混合物含有铜原子数一定为NA
C.标准状况下,5.6L O2作氧化剂时转移电子数一定为NA
D.500mL 2mol·L-1Na2CO3溶液中含C微粒总数一定为NA
查看答案和解析>>
科目: 来源: 题型:
有机物W( )常用于合成维生素类药物。下列与W相关说法正确的是
)常用于合成维生素类药物。下列与W相关说法正确的是
A.分子式为C6H9O3
B.分子中含有2种官能团
C.分子中含有6种不同化学环境的氢原子
D.水溶液中lmolW可与3molNaOH完全反应
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z、W在元素周期表中的位置如图所示,其中Y所处的周期序数与主族序数之和为8。下列说法错误的是
A.Z元素的氧化物对应水化物的酸性一定弱于W
B.四种元素中Z的原子半径和形成的离子半径均最大
C.X、Z、W中最简单气态氢化物稳定性最弱的是Z
D.X、Y、Z的原子均能与氢原子形成四原子分子
查看答案和解析>>
科目: 来源: 题型:
化学与生产和生活密切相关,下列说法正确的是
A.金属钠可以保存在煤油或酒精中,防止在空气中变质
B.石油的裂化和煤的干馏,都属于化学变化
C.等质量的葡萄糖和果糖在人体内完全氧化释放的能量相等
D.聚氯乙烯制品易造成白色污染,可采用焚烧法处理
查看答案和解析>>
科目: 来源: 题型:
氢溴酸在医药和石化工业上有广泛用途。如图所示是模拟工业制备氢溴酸粗产品并精制的流程:
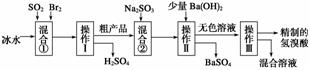
根据上述流程回答下列问题:
(1)混合①中发生反应的离子方程式为_______________________________________。
(2)混合①中使用冰水的目的是____________________________________________。
(3)操作Ⅲ一般适用于分离________混合物(填序号)。
a.固体和液体 b.固体和固体
c.互不相溶的液体 d.互溶的液体
(4)混合②中 加入Na2SO3的目的是__________________________________________。
加入Na2SO3的目的是__________________________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色。于是甲乙两同学设计了简单实验进行探究:
甲同学假设工业氢溴酸呈淡黄色是因为其中含有Fe3+,则用于证明该假设所用的试剂为________,若假设成立可观察到的现象为________________;乙同学假设工业氢溴酸呈淡黄色是因为其中含有______________________,其用于证明该假设所用的试剂为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com