
科目: 来源: 题型:
在恒温、恒容的密闭容器中进行反应A(g)≒B(g)+C(g)。若反应物的浓度由3 mol·L-1降到1.8 mol·L-1需30 s,那么反应物浓度由0.8 mol·L-1降至0.2 mol·L-1所需反应时间为( )
A. 15 s B. 大于15 s C. 小于15 s D. 无法判断
查看答案和解析>>
科目: 来源: 题型:
下列叙述中,正确的是( )
A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.两原子的核外电子排布相同,则一定属于同种元素
D.一种阳离子和一种阴离子的质子数和电子数可能同时相等
查看答案和解析>>
科目: 来源: 题型:
某实验小组设计用50 mL 1.0 mol/L盐酸跟50 mL 1.1 mol/L氢氧化钠溶液在如图所示装置中进行中和反应。在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过。通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
(1) 实验时氢氧化钠溶液的浓度要用0.55 mol/L的原因是_____________________________;实验中若改用60 mL 1.0mol/L的盐酸与50 mL 1.1mol/L的氢氧化钠溶液进行反应,与上述实验相比,所放出的热量______________(填“相等”或“不相等”),若实验操作均正确,则所求中和热_________________(填“相等”或“不相等”);
| 实验 序号 | 起始温度t1/℃ | 终止温度 (t2)/℃ | 温差 (t2-t1)/℃ | ||
| 盐酸 | NaOH 溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 31.8 | 6.7 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
(2)该实验小组做了三次实验,每次取溶液各50 mL,并记录如下原始数据。已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容c=4.18×10-3 kJ/(g·℃),则该反应的中和热为ΔH= _______。
(3)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会_________(填“偏大”、“偏小”或“不变”),其原因是__________________________________。
(4)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热____________(填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的 化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。
(1)a极是 极,b极是 极,电极反应式
分别为____________________________,
____________________________。
(2)这种电池的输出电压为1.2V。要使标有1.2V,1.5W的小灯泡连续发光0.5h,应消耗标准状况下的H2____________L。
(3)氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料,往往是某些碳氢化合物,如甲烷(天然气)、汽油等。请写出将图中H2换成CH4时所构成的甲烷燃料电池中a极的电极反应式:______________________________。
此时电池内总的反应方程式为 ______________________ 。
查看答案和解析>>
科目: 来源: 题型:
在400℃,1.01X105Pa时,将SO2和14molO2 压入一个装有催化剂的VL密闭反应器中,发生2SO2+O2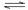 2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2
2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2
(1)SO2的起始浓度为_________,SO3(g)的平衡浓度为_________;
(2)SO2的转化率为_________,O2的平均反应速率为_________;
(3)平衡时SO3占总体积的百分数为________________,
此时体系压强为反应起始时体系压强的________倍;
(4)达平衡后再加入2molSO2、12molO2和4molSO3(g),此时正反应速率将__________,
逆反应速率将__________(填“增大”,“减小”或“不变”),平衡__________移动(填“向左”,“向右”或“不”)。
查看答案和解析>>
科目: 来源: 题型:
在火箭推进器中装有还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,并放出大量的热量。已知0.4mol液态肼和足量双氧水反应生成氮气和水蒸气时放出256.65KJ的热量。
(1).写出肼和过氧化氢的结构式, 肼________________,过氧化氢____________________。
(2).上述反应应用于火箭推进剂,除释放出大量热量和快速产生大量气体外,还有一个很突出的优点是__________________________________________。
(3).写出肼和双氧水反应的热化学方程式_____________________________。
(4).已知H2O(l)==H2O(g);△H= +44KJ/mol,则16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量是___________。
(5).已知N2(g) + 2O2(g) == 2NO2(g);△H= +67.7KJ/mol,
N2H4(g) + O2(g) == N2(g)+2H2O(g);△H= -534KJ/mol,
则肼与NO2完全反应的热化学方程式为_________________________________________。
查看答案和解析>>
科目: 来源: 题型:
已知在 25℃ ,101kPa 下,1g C8H18(辛烷)燃烧生成二氧化碳和液态水时放出48.40 kJ热量。表示上述反应的热化学方程式正确的是 ( )
A. C8H18(l) + 25/2 O2(g) = 8CO2(g)+ 9H2O(g);ΔH = - 48.40 kJ·mol-1
B. C8H18(l) + 25/2 O2(g) = 8CO2(g) + 9H2O(l);ΔH = - 5518 kJ·mol-1[
C. C8H18(l) + 25/2 O2(g) = 8CO2(g) + 9H2O(l);ΔH = + 5518 kJ·mol-1
D. C8H18(l) + 25/2 O2(g) = 8CO2(g) + 9H2O(l);ΔH = - 48.40 kJ·mol-1
查看答案和解析>>
科目: 来源: 题型:
相同容积的4个密闭容器中,进行同样的可逆反应:2A(g)+B(g) 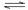 3C(g)+2D(g)。起始是,甲、乙、丙、丁4个容器所装A和B的量分别为:甲:A:2mol,B:1mol;乙:A:1mol,B:1mol;丙:A:2mol,B:2mol;丁:A:1mol,B:2mol。
3C(g)+2D(g)。起始是,甲、乙、丙、丁4个容器所装A和B的量分别为:甲:A:2mol,B:1mol;乙:A:1mol,B:1mol;丙:A:2mol,B:2mol;丁:A:1mol,B:2mol。
在相同温度下建立平衡时,A或B的转化率的大小关系为 ( )
A.A的转化率:甲<丙<乙 <丁 B. A的转化率:甲<乙<丙<丁
C. B的转化率:甲>丙>乙>丁 D. B的转化率:丁>乙>丙>甲
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、M、N代表五种金属,有以下化学反应:
①水溶液中:X + Y2+ = X2+ + Y②Z + 2H2O(冷) = Z(OH)2 + H2↑ ③M、N为电极与N盐溶液组成原电池,发生的电极反应为:M → M2+ + 2e- ④Y可以溶于稀H2SO4中,M不被稀H2SO4氧化
这五种金属的活动性由弱到强的顺序是 ( )
A.M<N<Y<X<Z B.N<M<X<Y<Z C.N<M<Y<X<Z D.X<Z<N<M<Y
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com