
科目: 来源: 题型:
【选做题】本题包括A、B 两小题,请选定其中一小题,并在相应的答题区域内作答。
若多做,则按A小题评分。
A.[物质结构与性质]
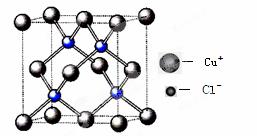
利用反应:Cu2Cl2 +C2H2+2NH3→Cu2C2(乙炔亚铜,红色)+2NH4Cl可检验乙炔。
(1)基态时亚铜离子核外电子排布式为 ▲ 。
(2)NH3中氮原子的杂化方式为 ▲ ;NH4+空间构型为 ▲ (用文字描述)。
(3)乙炔分子中σ键与π键数目之比为 ▲ ,与C22-互为等电子体的分子有 ▲ (写化学式,举一例)。
(4)氯化亚铜晶胞结构如下图,晶胞中含Cu+数目为 ▲ 。
(5)合成氨工业常用铜(I)氨溶液吸收CO生成[Cu(NH3)3(CO)]+,该配离子中配体有 ▲ (写化学式)。
B.[实验化学]
已二酸是一种重要的化工中间体,可通过氧化环已醇得到。
反应原理为:

实验步骤:
步骤1.在图①所示装置的三颈瓶中加入6gKMnO4和50mL0.3mol/LNaOH溶 液,搅拌加热使之溶解。
液,搅拌加热使之溶解。
步骤2.在继续搅拌下用滴管滴加21mL环已醇,控制滴加速度,维持反应温度43~47℃。滴加完毕后, 在沸水浴中将混合物加热几分钟。
在沸水浴中将混合物加热几分钟。
步骤3.用图②所示装置趁热抽滤,二氧化锰滤渣用水洗2~3次
步骤4.滤液用小火加热蒸发浓缩至原来体积的一半,冷却后再用浓盐酸酸化至pH为2~4,冷却析出粗产品
步骤5.将粗产品用水进行重结晶提纯,然后在烘箱中烘干。

(1)写出实验仪器名称:a ▲ ; b ▲ 。
(2)步骤2在沸水浴中将混合物加热几分钟的目的是: ▲ 。
(3)步骤3趁热抽滤的目的是: ▲ ;如 何证明步骤3滤渣已洗涤干净: ▲ 。
何证明步骤3滤渣已洗涤干净: ▲ 。
(4)步骤4用盐酸酸化的目的是: ▲ 。
(5)确定最后产品成分为已二酸,还需做的实验或仪器分析有 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
汽车在现代生活中扮演着越来越重要的角色,但其尾气(碳氢化合物、氮氧化物及一氧化碳等)带来的环境污染越来越明显,机动车废气排放已成为城市大气污染的重要来源。
(1)设汽油成分为C8H18,若在气缸中汽油高温裂解产生丁烷和丁烯,写出该反应的化学方程
▲ 。
(2)气缸中生成NO的反应为:N2(g)+O2(g)  2NO(g) △H >0
2NO(g) △H >0
①汽车启动后,气缸 内温
内温 度越高,单位时间内NO排放量越大,原因是 ▲ 。
度越高,单位时间内NO排放量越大,原因是 ▲ 。
②1mol空气中含有0.8molN2和0.2molO2,1300℃时在含1mol空气的密闭容器内反应达到平衡,测得NO为8×1 0-4mol。计算该温度下的平衡常数K≈ ▲ 。
0-4mol。计算该温度下的平衡常数K≈ ▲ 。
(3)尾气中的CO主要来自于汽油不完全燃烧。
①有人设想按下列反应除去CO:2CO(g)=2C(s)+O2(g) △H=+221kJ·mol-1,简述该设想能否实现的依据: ▲ 。
②测量汽车尾气的浓度常用电化学气敏传感器,其中CO传感器可用下图简单表示,则阳极发生的电极反应为 ▲ 。

(4)在汽车尾气系统中安装催化转换器,可有效减少尾气中的CO、NOx 和碳氢化合物等废气。
已知:N2(g)+O2(g)=2NO(g) △H1=+180kJ/mol
CO(g) +1/2O2(g)= CO2(g) △H2=-283kJ/mol
+1/2O2(g)= CO2(g) △H2=-283kJ/mol
2NO(g)+ 2CO(g) = 2CO2(g) + N2(g) △H3
则△H3 = ▲ kJ·mol-1。
(5)光化学烟雾(含臭氧、醛类、过氧乙酰硝酸酯等)是汽车尾气在紫外线作用下发生光化学反应生成的二次污染物。写出2-丁烯与臭氧按物质的量之比为1:2反应生成乙醛及氧气的化学方程式 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。
Ⅰ、制取氯化锌主要工艺如下:

下表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为
1.0 mol·L-1计算)。
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1. 1 | 3. 2 |
| Zn2+ | 5. 2 | 6. 4 |
| Fe2+ | 5. 8 | 8. 8 |
(1)加入H2O2溶液发生反应的离子方程式为 ▲ 。
(2)流程图中,为了降低溶液的酸度,试剂X可以是 ▲ (选填序号:a.ZnO;b.Zn(OH)2 ; c.Zn2(OH)2CO3 ;d.ZnSO4);pH应调整到 ▲ 。
(3)氯化锌能催化乳酸( )生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ▲ ,聚乳酸的结构简式为 ▲ 。
)生成丙交酯(C6H8O4)和聚乳酸,丙交酯的结构简式为 ▲ ,聚乳酸的结构简式为 ▲ 。
Ⅱ、制取金属锌采用碱溶解{ZnO(s)+2NaOH(aq)+H2O(l)=Na2[Zn(OH)4](aq)},然后电解浸取液。
(4)以石墨作电极电解时,阳极产生的气体为 ▲ ;阴极的电极反应为 ▲ 。
(5)炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
NaH2PO4、Na2HPO4可用于合成化工原料三聚磷酸钠(Na5P3O10)。
(1)能说明NaH2PO4溶液显弱酸性原因的离子方程式为 ▲ 。
(2)能说明Na2HPO4溶液显弱碱性原因的离子方程式为 ▲ 。
(3)测定某三聚磷酸钠试样中Na5P3O10的含量可用间接滴定法,其流程如下:

①滴定时所用的指示剂X可为 ▲ 。
②NaOH标准溶液应盛放在右上图所示的滴定管  ▲ (选填:“甲”或“乙”) 中。
▲ (选填:“甲”或“乙”) 中。
③滴定实验记录如下表(样品中杂质不与酸或碱反应)。
| 滴定次数 | 待测溶液A的体积(/mL) | 0.1000mol·L-1NaOH溶液的体积 | |
| 滴定前读数(/mL) | 滴定后读数(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
试计算样品中Na5P3O10的质量分数(列出计算过程,结果保留三位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
克百威是一种广谱内吸性杀虫剂,其合成路线如下图:
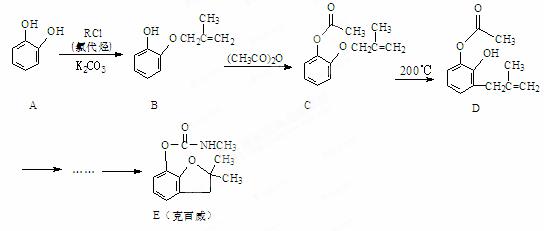
(1)试剂A容易变质,其可能的原因是 ▲ 。
(2)C中含氧官能团有 ▲ 和 ▲ (填名称)。
(3)B→C的反应类型为 ▲ 。
(4)克百威不能与碱性农药混合使用,其原因是 ▲ 。
(5)鉴别C和D两种异构体,最合适的试剂是 ▲ 。
(6)写出RCl的结构简式 ▲ 。
(7)写出满足下列条件的B的同分异构体的结构简式 ▲ (任写一种)。
①苯的衍生物 ②核磁共振氢谱有5组不同的峰 ③能发生银镜反应和水解反应
查看答案和解析>>
科目: 来源: 题型:
今有氧、镁、铝、硫、铬5种元素,试回答下列问题
(1)镁晶体堆积方式为 ▲ 堆积(选填:“简单立方”、“体心立方”、“面心立方”、“六方”);
(2)用“>”、“<”填写下表
| 第一电离能 | 电负性 | 晶格能 | 沸点 |
| Mg ▲ Al | O ▲ S | MgO ▲ MgS | H2O ▲ H2S |
(3)基态铬原子外围电子轨道表示式为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
在2L的密闭容器中,起始时均投入2molCO,在不同条件下发生反应:CO(g) +2H2(g)  CH3OH(g) △H <0。有关信息如图所示,下列说法正确的是
CH3OH(g) △H <0。有关信息如图所示,下列说法正确的是
A.T1<T2
 B.T1℃时该反应的平衡常数为4.0 L2·mol-2
B.T1℃时该反应的平衡常数为4.0 L2·mol-2
C.D.相同条件下n(H2)/n(CO)越大,CO和H2的转化率也越大
查看答案和解析>>
科目: 来源: 题型:
利用下图装置可实现在铜片上镀镍,下列有关说法不正确的是

A.a为正极,d极为铜片
B.甲池是燃料电池、乙池是电镀池
C.b极上发生的电极反应为:CH4+10OH――8e-=CO32-+7H2O
D.c极上发生的电极反应为: Ni2+ + 2e-= Ni
查看答案和解析>>
科目: 来源: 题型:
常温下,0.1mol·L-1NH4HCO3溶液的pH=7.8,该溶液中微粒浓度间关系正确的是
A.c(OH-)>c(H+)
B.c(HCO3-)>c(NH4+)
C.c(NH4+) + c(H+)= c(HCO3-) + 2c(CO32-) + c(OH-)
D.c(H2CO3) + c(H+) = c(CO32-) + 2c(NH3·H2O) + c( OH-)
OH-)
查看答案和解析>>
科目: 来源: 题型:
香茅醛是一种食用香精,异蒲勒醇是一种增香剂,一定条件下,香茅醛可转化为异蒲勒醇。下列说法不正确的是
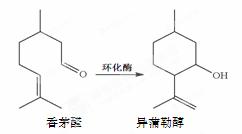
A.香茅醛与异蒲勒醇互为同分异构体
B.香茅醛的分子式为C10H19O
C.异蒲勒醇可发生加成、取代、消去反应
D.鉴别香茅醛与异蒲勒醇可用Br2水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com