
科目: 来源: 题型:
A、B两元素的原子分别得到2个电子形成稳定结构时,A放出的能量大于B放出的能量;C、D两元素的原子分别失去一个电子形成稳定结构时,D吸收的能量大于C吸收的能量。若A、B、C、D间分别形成化合物时,属于离子化合物可能性最大的是 ( )
A.D2A B.C2B C.C2A D.D2B
查看答案和解析>>
科目: 来源: 题型:
某元素的原子最外电子层排布是5s25p1,该元素或其化合物不可能具有的性质是 ( )
A.该元素单质是导体 B.该元素单质在一定条件下能与盐酸反应
C.该元素的氧化物的水合物显碱性 D.该元素的最高化合价呈+5价 ( )
查看答案和解析>>
科目: 来源: 题型:
据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报
道的认识正确的是 ( )
A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论
B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体
C.丙认为H3分子实质上是H2分子与H+ 以特殊共价键结合的产物,应写成H3+
D.丁认为如果上述的发现存在,则证明传统的价键理论有一定的局限性有待继续发展
查看答案和解析>>
科目: 来源: 题型:
某金属M的氢氧化物的水合晶体M(OH)2·xH2O与Na2CO3的混合物共36.800g,加入足量的水后,生成白色沉淀(该沉淀不含结晶水),将沉淀滤出,洗净烘干,称得其质量为9.850g。将得到的沉淀高温灼烧后,质量变为7.650g;滤液与酸作用不产生气体;若用足量的铵盐与滤液共热,则产生4.48L气体(标准状况)。求:
(1)滤液中OH-的物质的量?
(2)求M的相对原子质量。
(3)M的氢氧化物的水合晶体的化学式。
查看答案和解析>>
科目: 来源: 题型:
以石油裂解气为原料,通过一系列化学反应可得到重要的化工产品增塑剂G。
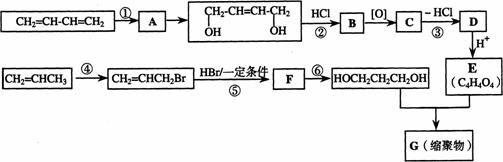
请完成下列各题:
(1)写出反应类型:反应① 反应④
(2)写出反应条件:反应③ 反应⑥
(3)反应②③的目的是: 。
(4)写出反应⑤的化学方程式: 。
(5)B被氧化成C的过程中会有中间产物生成,该中间产物可能是 (写出一种物质的结构简式)。
(5) 写出G的结构简式 。
查看答案和解析>>
科目: 来源: 题型:
已知一个碳原子上连有两个羟基时,其结构极不稳定,易发生下列变化,生成较稳定物质:如: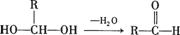
A-F是六种有机化合物,它们之间的关系如下图,请根据要求回答:
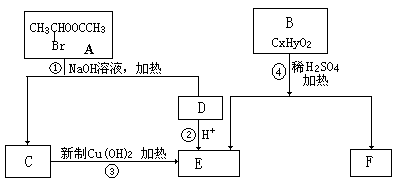

(1)物质C的结构简式 ,物质D的结构简式 ;
(2)反应③的化学方程式为 .
(3)已知B的相对分子质量为162,其完全燃烧的产物中n(CO2):n (H2O)=2:1。F是高分子光阻剂生产中的主要原料。F具有如下特点:①能跟FeCl3溶液发生显色反应;②能发生加聚反应;③苯环上的一氯代物只有两种。F在一定条件下发生加聚反应的化学方程式为 。
(4) 化合物G是F的同分异构体,属于芳香族化合物,能发生银镜反应。G有 种
查看答案和解析>>
科目: 来源: 题型:
海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。

完成下列填空:
(1)氯碱工业主要以食盐为原料。为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列操作,正确的操作顺序是 。
①过滤 ②加过量的NaOH溶液 ③加适量的盐酸 ④加过量的Na2CO3溶液
⑤加过量的BaCl2溶液
a.②⑤④①③ b.①④②⑤③ c.④②⑤③① d.⑤②④①③
(2)在实验室中可以用萃取的方法提取溴,可选用的试剂是________________,所用主要仪器的名称是____________________。
(3)步骤Ⅰ中用硫酸酸化可提高Cl2利用率的原因是 。
(4)步骤II反应的离子方程式__________________________________________。
(5)Mg(OH)2沉淀中混有Ca(OH)2,可选用__________溶液进行洗涤除去。
查看答案和解析>>
科目: 来源: 题型:
25℃时,在一体积为2L的密闭容器中,气态物质A、B、C的物质的量n(mol)随时间t的变化如下图所示。已知达平衡后,降低温度,A的转化率增大。

(1)根据上图数据,从反应开始到达第一次平衡时的平均速率v(A)为 。
(2)在25℃时,达到第一次平衡,则此反应的方程式为 。
(3)在5~7min内,若温度不变,则此处曲线变化的原因是 。
查看答案和解析>>
科目: 来源: 题型:
元素周期表反映了元素性质的周期性变化规律。请根据元素性质及题给信息回答下列问题:
⑴下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关性质相符的曲线标号填入相应的空格中:
①ⅡA族元素的最高正化合价 ;
②第三周期主族元素的最高价氧化物对应水化物的碱性 ;

⑵某同学得到两张有关几种短周期元素信息的表格:
表一
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
表二
| 元素代号 | 元素特征信息 |
| A | 其单质是密度最小的物质。 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一。 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B元素可以形成两种以上的离子化合物。 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,原子半径在该周期最小 |
①上述两张表格中,指的是同种元素的是__________________________。(填元素代号)
②在两张表格中,非金属性最强的元素原子的电子排布式为 ;金属性最强的元素位于周期表的第 周期 族。
③写出A、B、C形成的化合物的电子式
④在短周期主族元素中,E元素及与其相邻元素的原子半径从大到小的顺序是
(用元素符号表示)。
⑤QT2形成的化合物在固态时为_________晶体。
⑥请写出一个能说明D与L金属性强弱的事实______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com