
科目: 来源: 题型:
将含有0.400 mol Cu(NO3)2和0.400 mol KCl的水溶液1.00 L,用惰性电极电解一段时间后,在一个电极上析出0.300 mol Cu,此时在另一电极上放出的气体在标准状况下的体积为
A.3.36L B.6.72L
C.5.60L D.大于5.60L,小于6.72L
查看答案和解析>>
科目: 来源: 题型:
用惰性电极电解某溶液时,发现两极只有H2和O2生成,若电解前后温度变化忽略不计,则电解一段时间后,下列有关溶液叙述正确的有
①该溶液的pH可能增大②该溶液的pH可能减小③该溶液的pH可能不变④该溶液的浓度可能增大⑤该溶液的浓度可能减小⑥该溶液的浓度可能不变
A.①②③④⑤⑥ B.①②③④⑤
C.①②③④⑥ D.①②③④
查看答案和解析>>
科目: 来源: 题型:
已知:2CrO42-(黄色)+2H+  Cr2O72-(橙色)+H2O。现以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下(阳离子交换膜只允许阳离子通过):
Cr2O72-(橙色)+H2O。现以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如下(阳离子交换膜只允许阳离子通过):
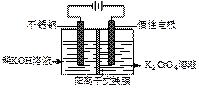
下列说法不正确的是
A.在阴极室,发生的电极反应为:2H2O+2e-=2OH-+H2↑
B.在阳极室,通电后溶液逐渐由黄色变为橙色,是因为产生的H+,与CrO42-离子反应使2CrO42-+2H+  Cr2O72-+H2O向右进行
Cr2O72-+H2O向右进行
C.该制备过程总反应的化学方程式为:
4K2CrO4+4H2O 2K2Cr2O7+4KOH+2H2↑+O2↑
2K2Cr2O7+4KOH+2H2↑+O2↑
D.测定阳极液中K和Cr的含量,若K与Cr的物质的量之比(nK/nCr )为d,则此时铬酸钾的转化率为1-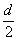
查看答案和解析>>
科目: 来源: 题型:
关于下列各装置图的叙述中,不正确的是
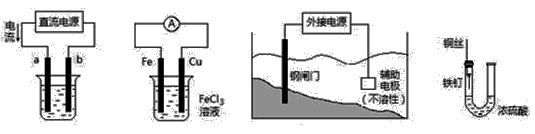
① ② ③ ④
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.装置②的总反应是:Cu+2Fe3+= Cu2++2Fe2+
C.装置③中钢闸门应与外接电源的负极相连
D.装置④中的铁钉几乎没被腐蚀
查看答案和解析>>
科目: 来源: 题型:
已知电极上每通过96 500 C的电量就会有1 mol电子发生转移。精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量。实际测量中,常用银电量计,如图所示。下列说法不正确的是

A.电量计中的银棒应与电源的正极相连,铂坩埚上发生的电极反应是:Ag++e-= Ag
B.称量电解前后铂坩埚的质量变化,得金属银的沉积量为108.0 mg,则电解过程中通过电解池的电量为96.5 C
C.实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋。若没有收集网袋,测量结果会偏高。
D.若要测定电解饱和食盐水时通过的电量,可将该银电量计中的银棒与待测电解池的阳极相连,铂坩埚与电源的负极相连。
查看答案和解析>>
科目: 来源: 题型:
三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,再加入适量硫酸钠后进行电解。电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍。以下说法不正确的是
A.可用铁作阳极材料
B.电解过程中阳极附近溶液的pH降低
C.阳极反应方程式为:2Cl--2e-=Cl2
D.1 mol二价镍全部转化为三价镍时,外电路中通过了1 mol电子
查看答案和解析>>
科目: 来源: 题型:
(1)甲烷通常用来作燃料,其燃烧反应的化学方程式是 。
(2) 若用甲烷—氧气构成燃料电池,电解质溶液为KOH溶液,试写出该电池的
正极的电极反应式 ;
负极的电极反应式 。
查看答案和解析>>
科目: 来源: 题型:
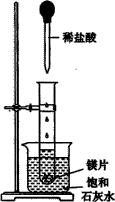 除标明外,其余每空2分)如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中。试回答下列回答:
除标明外,其余每空2分)如图所示,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中。试回答下列回答:
(1)实验中观察到的现象是____________________。(选填代号,3分)
A.试管中镁片逐渐溶解
B.试管中产生无色气泡
C.烧杯外壁变冷
D.烧杯底部析出少量白色固体
(2)试管中发生的反应属于_______________(选填“氧化还原反应”或“非氧化还原反应”)。
(3)写出有关反应的离子方程式________________。
(4)由实验推知,MgCl2溶液和H2的总能量________(填“大于”“小于”“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目: 来源: 题型:
往一个容积为5L的密闭容器中,通入2molN2和3molH2,在一定条件下,发生反应 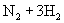

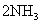 ,2 min后,测得容器中生成了1mol NH3,试求:
,2 min后,测得容器中生成了1mol NH3,试求:
(1)2 min时,N2的物质的量 ;
(2) 2 min时,H2的物质的量浓度 ;
(3)2 min时,H2的转化率 ;
(4)2min内,N2的平均反应速率 ;
(5)N2、H2、NH3的反应速率之比 。
查看答案和解析>>
科目: 来源: 题型:
实验室利用如右图装置进行中和热的测定。
 回答下列问题:
回答下列问题:
①如图装置中,为了酸碱能更充分地反应,应该增加一个 (填玻璃仪器名称);大烧杯上没有盖上硬纸板,测得的中和热数值将会
(填“偏大”、“偏小”或“无影响”)。
②在操作正确的前提下提高中和热测定的准确性的关键是 ( 填代号)
A.进行实验时的气温
B.装置的保温隔热效果
C.实验所用酸碱溶液的体积
③如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将 (填“偏大”、“偏小”、“不变”);原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com