
科目: 来源: 题型:
对已达平衡的下列反应2X(g)+Y(g)2Z(g),减小压强时,对反应产生的影响是( )
A、逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B、逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C、正、逆反应速率都减小,平衡向逆反应方向移动
D、正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
对可逆反应X+Y Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则图象中关于X、Y、Z、W四种物质的聚集状态正确的说法为( )
Z+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图所示,则图象中关于X、Y、Z、W四种物质的聚集状态正确的说法为( )
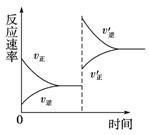
A、Z、W均为气体,X、Y中有一种是气体
B、Z、W中有一种是气体,X、Y皆非气体
C、X、Y、Z、W皆非气体
D、X、Y均为气体、Z、W中有一种为气体
查看答案和解析>>
科目: 来源: 题型:
以下关于化学反应速率的说法正确的是( )
A、化学反应速率可用某时刻生成物的质量增加来表示
B、在同一反应中,用各种物质表示的化学反应速率的大小相等
C、化学反应速率指单位时间内反应物浓度的减少或生成物浓度的增加
D、若反应现象在短时间内出现,则反应速率快,若无明显现象,则反应速率慢
查看答案和解析>>
科目: 来源: 题型:
请从下图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生氢气的体积(大于25 mL),并检验氯气的氧化性。

(1)A极发生的电极反应式是______ ____________________________,
____________________________,
B极发生的电极反应式是__________________________________________。
电解饱和食盐水的化学方程式____________________________________________。
(2)电源、电流表与A、B两极的正确连接顺序为:
L→( )→( )→( )→( )→M。
(3)设计上述气体实验装置时,各接口的正确连接顺序为:________接________、________接A、B接________、________接________。
(4)在实验中,盛有KI淀粉溶液的容器中发生反应的离子方程式为______________。
(5)已知饱和食盐水50 mL,某时刻测得H2体积为5.6 mL(标准状况)。此时溶液pH约为__________________。
查看答案和解析>>
科目: 来源: 题型:
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。

请回答:
(1)B极是电源的______________,一段时间后,甲中溶液颜色________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明___________________,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为________。
(3)现用丙装置给铜件镀银,则H应是________________(填“镀层金属”或“镀件”),电镀液是________溶液。当乙中溶液的pH是13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生的总反应的离子方程式为:________________________。
查看答案和解析>>
科目: 来源: 题型:
钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。请回答钢铁腐蚀与防护过程中的有关问题。

(1)钢铁的电化学腐蚀原理如图所示:
①写出石墨电极的电极反应式__________________________________________;
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在右图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向。
③写出修改后石墨电极的电极反应式_________________________________。
(2)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式_____________ ________________________。
________________________。
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下:

①A电极对应的金属是________(写元素名称),B电极的电极反应式是________________________。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则 电镀时电路中通过的电子为________ mol。
电镀时电路中通过的电子为________ mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是________________________(用离子方程式表示)。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的________。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为______________________。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是____________________________________________。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是______________。
 (3)利用右图装置,可以模拟铁的电化学防护。
(3)利用右图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于________处。若X为锌,开关K置于M处,该电化学防护法称为________。
查看答案和解析>>
科目: 来源: 题型:
 如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊溶液。下列实验现象中正确的是( )
如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加一滴石蕊溶液。下列实验现象中正确的是( )
A.逸出气体的体积: a电极的大于b电极的
a电极的大于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组的同学用如图所示装置研究电化学问题。当闭合该装置的电键时,观察到电流计的指针发生偏转。下列有关说法不正确的是
( )
A.甲装置是原电池,乙装置是电解池
B.当甲中产生0.1 mol气体时,乙中析出固体的质量为3. 2 g
C.实验一段时间后,甲烧杯中溶液的pH增大
D.将乙中的C电极换成铜电极,则乙装置可变成电 镀装置
镀装置
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.铅蓄电池放电时铅电极发生氧化反应
B.电解饱和食盐水在阳极得到氯气,阴极得到金属钠
C.给铁钉镀铜可采用CuSO4作电镀液
D.生铁浸泡在食盐水中发生析氢腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com