
科目: 来源:不详 题型:单选题
| A.选择仪器时,使用500mL容量瓶 |
| B.将称量好的氢氧化钠固体放入容量瓶中,加入少量水溶解 |
| C.在烧杯中溶解氢氧化钠固体后,立即将所得溶液注入容量瓶中 |
| D.将烧杯中的氢氧化钠溶液注入未经干燥的洁净容量瓶中 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.所用固体NaOH已潮解 |
| B.定容时仰视刻度 |
| C.用带游码的托盘天平称2.4gNaOH时,误把砝码放在了左边 |
| D.配制完毕,不小心溅出几滴溶液,为使溶液的浓度不减少,又在配好的溶液中加入少量的NaOH固体 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
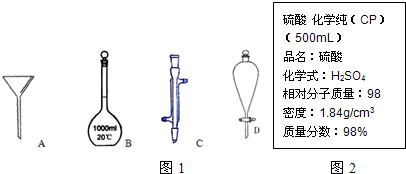
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com