
科目: 来源: 题型:
为验证氧化性Cl2 > Fe3+ > SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。

实验过程:
I. 打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ. 打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ. 当B中溶液变黄时,停止加热,关闭K2。
Ⅳ. 打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ. 打开K3和活塞c,加入70%的硫酸,一段时间后关闭K3。
Ⅵ. 更新试管D,重复过程Ⅳ,检验B溶液中的离子。
⑴过程Ⅰ的目的是 。
⑵棉花中浸润的溶液为 。
⑶A中发生反应的化学方程式 。
⑷若将制取的SO2通入酸性高锰酸钾溶液可使溶液褪色,其离子方程式为 。
⑸甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性Cl2 > Fe3+ > SO2的是 (填“甲”“乙”“丙”)。
| 过程Ⅳ B溶液中含有的离子 | 过程Ⅵ B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目: 来源: 题型:
某化学兴趣小组利用某废弃的氧化铜锌矿制取活性ZnO实验流程如下:

请回答下列问题:
⑴加入铁粉后发生反应的离子方程式为_________________________,_______ _。
⑵甲、乙两同学选用下列仪器,采用不同的方法制取氨气。
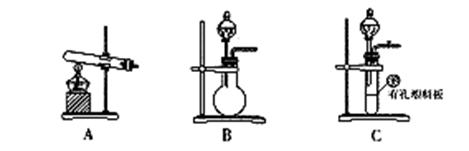
①甲同学使用的药品是熟石灰与氯化铵,则应选用装置_______(填写装置代号),生成氨气的化学方程式为_______________________________________;
②乙同学选用了装置B,则使用的两种药品的名称为______________ _。
⑶H2O2的作用是____________________________________________________。
⑷除铁过程中得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂(K2FeO4),该反应中氧化剂与还原剂的物质的量之比为____________。
⑸已知溶液a中含有CO2- 3、SO2- 4两种酸根阴离子,若只允许取用一次样品,检验这种离子存在的实验操作过程为_____________________________
查看答案和解析>>
科目: 来源: 题型:
中学常见的某反应的化学方程式为A+B→C+D+H2O(未配平,反应条件略去)。
请回答下列有关问题。
⑴若A是铁,B是稀硝酸(过量),且A可溶于C溶液中。则A与C反应的离子方程式为__________________________________________________。
⑵若C、D均为气体,且都能使澄清石灰水变浑浊,某探究性学习小组利用下图中所列装置设计实验,证明上述反应中有C、D生成。
[&X&X&K] 
则B瓶溶液的作用是________ _,装置D中所盛溶液是_______ _,若要验证另一产物水的存在,需使用的药品为_______ __,该装置在整套装置中的位置是_________ _。
⑶若C是无色有刺激性气味的气体,其水溶液呈弱碱性。写出C发生催化氧化反应的化学方程式_______________________________________________________。
⑷若D为氯碱工业的主要原料,C是造成温室效应的主要气体之一,则上述的反应的化学方程式为______________________________。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相对位置如图,A元素最外层与次外层上的电子数之差为3,B为地壳中含最最多的金属元素。
⑴D离子结构示意图为_____________。
| A | |
| C |
⑵将C的低价态氧化物甲通入到D单质的水溶液会使之褪色,写出该反应的离子方程式
____________________ _。
⑶A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100 mL 8.0 mol/L乙的浓溶液中,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是_________,还原剂失电子数为_________________。
⑷将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为_________,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为_____________________________________;B单质表面的氧化膜可用NaOH溶液除去,写出该反应的化学方程式____________________ _。
查看答案和解析>>
科目: 来源: 题型:
C和CuO在一定温度下反应,产物有Cu、Cu2O、CO、CO2。若将2.00 g C跟16.0 g CuO混合,隔绝空气加热,将生成的气体全部通过足量的澄清石灰水,反应一段时间后共收集到1.12 L气体(标准状况),生成沉淀的质量为5.00 g。下列说法错误的是( )
A.反应后的固体混合物中Cu的质量为12.8 g
B.反应后的固体混合物中还含有碳
C.反应后的固体混合物总质量为13.6 g
D.反应后的固体混合物中氧化物的物质的量为0.05mol
查看答案和解析>>
科目: 来源: 题型:
水溶液X中只可能溶有K+、Mg2+、Al3+、AlO2-、SiO32- 、SO32-、CO32- 、SO42-中的若干种离子。某同学对该溶液进行了如下实验:

下列判断错误的是( )
A.气体甲可能是混合物
B.沉淀甲是硅酸和硅酸镁的混合物
C.白色沉淀乙的主要成分是氢氧化铝[学科
D.K+、AlO2-和SiO32-一定存在于溶液X中
查看答案和解析>>
科目: 来源: 题型:
下列表述或化学用语书写正确的是( )
A.向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:
Ba2++OH-+H++SO2- 4=BaSO4↓+H2O
B.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑
C.FeSO4溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+=2Fe3++2H2O
D.金属铝与氧化镁发生铝热反应:2Al+3MgO 高温 3Mg+Al2O3
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数的值,下列说法中正确的是( )
A.62 g Na2O溶液于水后所得溶液中含有的O2-数为NA
B.标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA
C.常温常压下,16g甲烷(12C1H4)所含的中子数为10NA
D.常温常压下,14g由N2和CO组成的混合气体含有的原子数目为NA
查看答案和解析>>
科目: 来源: 题型:
将4.6 g Cu和Mg完全溶于浓硝酸溶液中,反应中硝酸的还原产物为4480mL NO2气和336 mL N2O4气体(标准状况下),反应后的溶液中,加入过量NaOH溶液,生成沉淀的质量为 ( )
A. 9.02 g B. 8.51 g C. 8.26 g D. 7.04 g
查看答案和解析>>
科目: 来源: 题型:
在给定条件下,下列加点的物质在化学反应中完全消耗的是( )
A.用50mL 12 mol·L-1的氯化氢水溶液与足量二氧化锰共热制取氯气
B.将1g铝片投入20mL 18.4 mol·L-1的硫酸中
C.向100mL 3 mol·L-1的硝酸中加入5.6g铁
D.常温常压下,0.1mol氯气通入1L水中反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com