
科目: 来源:郑州一模 题型:填空题
查看答案和解析>>
科目: 来源:江西模拟 题型:填空题
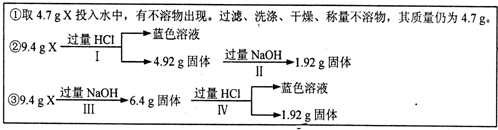
查看答案和解析>>
科目: 来源:不详 题型:问答题
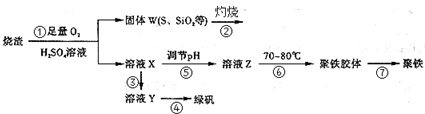
查看答案和解析>>
科目: 来源:不详 题型:问答题
| ①镁、铝、锌都是银白色的金属 ②锌(Zn)可以与NaOH溶液反应生成H2 ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3?H2O ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸分解生成Zn2+、NH4+ |

查看答案和解析>>
科目: 来源:枣庄模拟 题型:问答题


查看答案和解析>>
科目: 来源:不详 题型:问答题
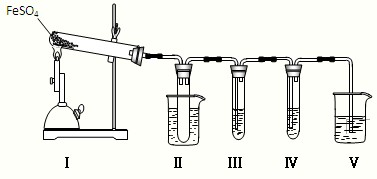
| 检验试剂 | 预期现象和结论 |
| 装置Ⅲ的试管中加入______. | 产生大量白色沉淀,证明气体产物中含有SO3. |
| 装置Ⅳ的试管中加入______. | ______ |
查看答案和解析>>
科目: 来源:枣庄模拟 题型:问答题
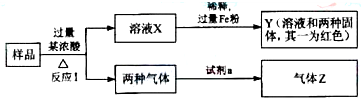
查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:不详 题型:填空题

查看答案和解析>>
科目: 来源:深圳二模 题型:问答题
| 所加试剂 | 预期现象和结论 |
| 试管A中加足量① ; 试管B中加1%品红溶液; 试管C中加② . |
若A中溶液变蓝色,B中溶液不退色,C中溶液变浑浊.则消毒液部分变质; ③ 则消毒液未变质; ④ 则消毒液完全变质. |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com