
科目: 来源:不详 题型:单选题
| A.可以推算出该有机物的化学式 |
| B.分子中C、H原子个数之比为1:2 |
| C.分子中C、H原子个数之比为1:1 |
| D.分子中必定含氧原子 |
查看答案和解析>>
科目: 来源:不详 题型:填空题
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 没有现象发生 |
| ② | B+D | 有气体放出 |
| ③ | B+C | 有沉淀生成 |
| ④ | A+D | 有沉淀生成 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| ① | ② | ③ | |
| (A) | BaCl2 | HNO3 | Na2SO4 |
| (B) | CaCl2 | HNO3 | KCl |
| (C) | KCl | H2SO4 | CaCl2 |
| (D) | BaCl2 | H2SO4 | CaCl2 |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目: 来源:广东省模拟题 题型:实验题

查看答案和解析>>
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:河北省期末题 题型:实验题

查看答案和解析>>
科目: 来源:0103 月考题 题型:实验题

查看答案和解析>>
科目: 来源:西城区模拟 题型:填空题
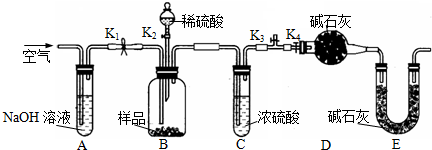
查看答案和解析>>
科目: 来源:同步题 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com