
科目: 来源: 题型:
将1L含有0.4mol CuSO4和0.2mol NaCl的水溶液用惰性电极电解一段时间后,若在一个电极上得到0.3mol Cu,则:
求:(1)另一电极上析出气体(在标准状况下)的体积是多少?
(2)此时溶液的H+离子浓度是多少?(溶液体积变化不计)
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组为了研究影响化学反应速率的因素,设计如下方案:
| 实验编号 | 0.01mol•L﹣1 酸性KMnO4溶液 | 0.1mol•L﹣1 H2C2O4溶液 | 水 | 1mol•L﹣1 MnSO4溶液 | 反应温度/℃ | 反应时间 |
| I | 2ml | 2ml | 0 | 0 | 20 | 125 |
| II | ▲ | ▲ | 1ml | 0 | 20 | 320 |
| III | ▲ | ▲ | ▲ | 0 | 50 | 30 |
| IV | 2ml | 2ml | 0 | 2滴 | 20 | 10 |
反应方程式:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O
(1)实验计时方法是从溶液混合开始记时,至 ▲ 时记时结束。
(2)实验I和II研究浓度对反应速率的影响,实验I和III研究温度对反应速率的影响.请在上表空格中填入合理的实验数据.
(3)从实验数据分析,实验I和IV研究 ▲ 对反应速率的影响.
查看答案和解析>>
科目: 来源: 题型:
已知有一种节能的氯碱工业新工艺,将电解池和燃料电池相组合,相关流程如下图所示(电极未标出):回答下列有关问题:
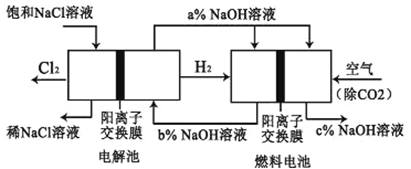
(1)燃料电池的正极反应式为 ________ _▲ ____ _;
燃料电池中阳离子的移动方向_______▲____(“从左向右”或“从右向左”)。
(2)电解池中阳离子交换膜的作用(写出两点) ▲
(3)电解池中产生2 mol Cl2,理论上燃料电池中消耗__▲___ mol O2。
(4)a、b、c的大小关系为:_____▲_____。
查看答案和解析>>
科目: 来源: 题型:
一定温度下,某密闭容器中充入等物质的量的气体A和B,发生如下反应:A(g)+xB(g)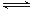 2C(g)。达到平衡后,只改变反应的一个条件,测得容器内有关物质的浓度、反应速率随时间的变化如下图所示。请回答下列问题:
2C(g)。达到平衡后,只改变反应的一个条件,测得容器内有关物质的浓度、反应速率随时间的变化如下图所示。请回答下列问题:
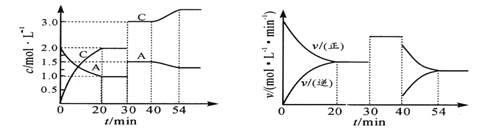
(1)在该条件下,当V(B)正 : V(C)逆 = ▲ 时反应达到了化学平衡状态。
(2)若25min、35min时的化学平衡常数分别为K1、K2,则二者的大小关系是 ▲ 。
(3)在甲、乙、丙三个相同的密闭容器中按表中所述投料,在恒温、恒容的条件下进行反应,平衡后测得A的浓度如表中所示:
| 容器 | 甲 | 乙 | 丙 |
| 起始投料 | 1molA和1molB | 2molC | 2molA和2molB |
| A的平衡浓度 | C1 | C2 | C3 |
则:C1、C2、C3三者数值的关系式为 ▲ (用代数式表示)
查看答案和解析>>
科目: 来源: 题型:
已知A(g)+B(g)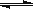 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| |温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ▲ ,△H ▲ 0(填“<”“ >”“ =”);
(2) 830℃时,向一个 5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol·L-1·s-1。,则6s时c(A)= ▲ mol·L-1,C的物质的量为 ▲ mol;反应经一段时间后达到平衡,此时A的转化率为 ▲ ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为 ▲ ;
(3)判断该反应是否达到平衡的依据为 ▲ (填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c. c(A)不随时间改变 d.单位时间里生成C和A的物质的量相等
(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为 ▲ 。
A(g)+B(g)的平衡常数的值为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
新型燃料逐渐取代传统燃料在工业生产和国防建设中广泛应用,回答下列问题:
(1)已知下列热化学方程式:
2H2(g)+O2(g)==2H2O(g) △H=-483.6 KJ.mol-1
H2O(l)==H2O(g) △H=+44 KJ.mol-1
则氢气的标准燃烧热 ▲ ,氢气热值 ▲ 。
(2)0.3mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ的热量。写出该反应的热化学方程式 ▲ 。
(3)肼可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气。
已知:①N2(g)+2O2(g)= N2O4 (1) △H1= -195kJ·mol-1
② N2H4(1) + O2(g)= N2(g) + 2H2O(g) △H2= -534.2kJ·mol-1
写出肼和N2O4反应的热化学方程式 ▲ 。
(4)肼一空气燃料电池是一种碱性电池,该电池放电时,负极的电极反应式为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
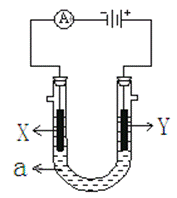
电解原理在化学工业中有广泛应用。右图表示一个电解池,装有电解液a ;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
⑴ 若X、Y都是惰性电极,a是Na2SO4溶液,
总反应方程式: ▲ ;
⑵ 若要在铁制品上镀上一层银
① X电极材料是 ▲ (填铁或银);② a是 ▲ 溶液
③ Y电极反应方程式: ▲ ;
⑶ 若X、Y都是铂电极,电解某金属的氯化物(XCl2)溶,当收集到1.12 L氯气时(标准状况),阴极增重3.2 g .
① 该金属的相对原子质量是 ▲ ;② 电路中有 ▲ mol电子通过。
查看答案和解析>>
科目: 来源: 题型:
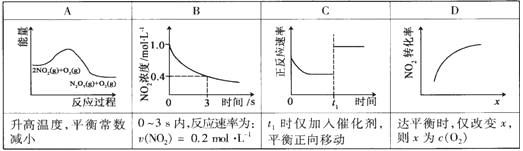
臭氧是理想的烟气脱硝试剂,其脱硝反应为:2NO2(g)+O3(g) N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
查看答案和解析>>
科目: 来源: 题型:
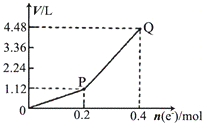
用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如右图所示。横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况)。下列判断正确的是 ( )
A.电解过程中,溶液的pH不断增大
B.当转移0.4mol e-时,电解生成的铜为6.4g。
C.阳极电极反应式为2H2O + 4e-=4H++O2↑
D.Q点对应的气体中,H2与O2的体积比为2:1
查看答案和解析>>
科目: 来源: 题型:
在恒温恒压的密闭容器中,充入 4L X和 3L Y的混合气体,在一定条件下发生下列反应:
4X(g)+ 3Y(g)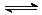 2Q(g)+ nR(g)达到平衡时测得 X的转化率为 25%,此时混和
2Q(g)+ nR(g)达到平衡时测得 X的转化率为 25%,此时混和
气体的体积为6.5L。则该反应方程式中的n值为: ( )
A.8 B.6 C.5 D.3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com