
科目: 来源: 题型:
己烯雌酚是一种激素类药物,其结构简式如下图所示。下列有关叙述中不正确的是
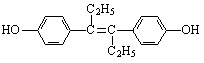 A.己烯雌酚的分子式为C18H20O2
A.己烯雌酚的分子式为C18H20O2
B.己烯雌酚分子中一定有16个碳原子共平面
C.己烯雌酚为芳香族化合物
D.己烯雌酚可发生加成、取代、氧化、加聚、酯化、硝化反应
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A.NaHCO3溶液加水稀释,c(Na+)/c(HCO3-)的比值保持增大
B.1 mol·L-1的NH4Cl溶液中含有NH4+的数目一定小于NA
C.用石墨电极电解FeCl3溶液,阴极反应:2Fe3++6H2O+6e-=2Fe(OH)3↓+3H2↑
D.将带有相反电荷的胶体混合,一定会出现胶体聚沉现象
查看答案和解析>>
科目: 来源: 题型:
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
A.微粒X2-与Y2+核外电子排布相同,离子半径:X2-> Y2+
B.人们可在周期表的过渡元素中寻找催化剂、耐腐蚀和耐高温的合金材料
C.由水溶液的酸性:HCl>HF,可推断出元素的非金属性:Cl>F
D.Be元素与Al元素同处在周期表的金属与非金属的交界处,可推出:
Be(OH)2+ 2OH-=BeO22-+2H2O
查看答案和解析>>
科目: 来源: 题型:
下表中的实验操作能达到实验目的或能得出相应结论的是
| 选项 | 实验内容 | 实验目的或实验结论 |
| A | 向盛有2 mL 0.1 mol/L AgNO3溶液的试管中滴加5滴0.1 mol/L NaCl溶液,有白色沉淀生成,再向其中滴加5滴0.1 mol/L KI溶液 | 说明一种沉淀能转化为溶解度更小的沉淀 |
| B | 向1 mL 20% 的蔗糖溶液中加入3~5滴稀硫酸,水浴加热5 min,冷却后再加入新制Cu(OH)2悬浊液,加热 | 证明蔗糖能发生水解反应[m] |
| C | 水浴加热浓硝酸、浓硫酸和苯的混合物后,直接蒸馏分液后得到的粗产品 | 制备纯硝基苯 |
| D | 室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入等体积不同浓度的稀硫酸 | 研究浓度对反应速率的影响 |
查看答案和解析>>
科目: 来源: 题型:
化学与生产、生活、社会密切相关。下列有关说法中不正确的是
A.航天服材质是由碳化硅、陶瓷和碳纤维等复合而成,它是一种新型无机非金属材料
 B.
B. 是放射性警示的标志
是放射性警示的标志
C.雾霾天气对人的健康造成危害,“雾”和“霾”的分散质微粒不相同
D.煤的主要成分为单质碳、苯、二甲苯等,因而可通过煤的干馏将它们分离
查看答案和解析>>
科目: 来源: 题型:
在容积为1L的密闭容器中,进行如下反应:A(g)+2B(g)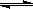 C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
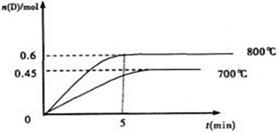
(1)800℃时。0—5min内,以B表示的平均反应速率为
(2)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中c(A)不变
C.2v正(B)=v逆(D) D.c(A)=c(C)
(3)若最初加入1.0molA和2.2molB,利用图中数据计算800℃时的平衡常数K= ,
该反应为 反应(填吸热或放热)
(4)700℃时,某时刻测得体系中各物质的量如下:n(A)=1.1mol,n(B)=2.6mol,n(C)=0.9mol, n(D)=0.9mol,则此时该反应 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)
查看答案和解析>>
科目: 来源: 题型:
研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s) + 3C(石墨) = 2Fe(s) + 3CO(g) △H 1 = +489.0 kJ·mol-1
C(石墨) +CO2(g) = 2CO(g) △H2 = +172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为 。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K= 。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应。反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图10所示,则该反应的ΔH 0(填“>”、“<”或“=”)。
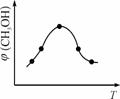
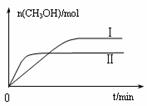
图10 图11
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图11所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ KⅡ(填“>”、“<”或“=”)。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为 。当氨碳比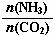 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为 。
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为 。
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为  。
。
查看答案和解析>>
科目: 来源: 题型:
可逆反应N2+3H22NH3是工业上合成氨的重要反应。
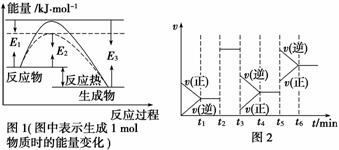
(1)根据图1请写出合成氨的热化学方 程式__________________________________(热量用E1、E2或E3表示)。
程式__________________________________(热量用E1、E2或E3表示)。
(2)图1中虚线部分是通过改变化学反应中的________条件,该条件的改变与图2中哪一时刻条件的改变相同________(用“t1~t6”表示)。
(3)t3时刻改变的条件是____________, t5时刻改变的条件是____________。
t5时刻改变的条件是____________。
查看答案和解析>>
科目: 来源: 题型:
在一个容积固定为2 L的密闭容器中,发生反应aA(g)+bB(g) pC(g) ΔH=?,反应情况记录如表:
pC(g) ΔH=?,反应情况记录如表:
| 时间 | c(A) (mol·L-1) | c(B) (mol·L-1) | c(C) (mol·L-1) |
| 0 | 1 | 3 | 0 |
| 第2 min[ | 0.8 | 2.6 | 0.4 |
| 第4 min | 0.4 | 1.8 | 1.2 |
| 第6 min | 0.4 | 1.8 | 1.2 |
请仔细分析,根据表中数据,回答下列问题:
(1)a=________,b=________,p=________。(取最小正整数)
(2)第2 min到第4 min内A的平均反应速率v(A)=________ mol·L-1·min-1。
(3)若从开始到第 4 min建立平衡时反应放出的热量为235.92 kJ,则该反应的ΔH=________。
4 min建立平衡时反应放出的热量为235.92 kJ,则该反应的ΔH=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com