
科目: 来源: 题型:
下列说法正确的是 ( )
①正常雨水的PH为7.0,酸雨的PH小于7.0。
②严格执行机动车尾气排放标准有利于防止大气污染
③使用二氧化硫和某些含硫化合物进行增白的食品会对人体健康产生损害
④使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害
⑤食品厂产生的含丰富氮、磷营养素的废水可长期排向水库养鱼
A、①②③ B、①④⑤ C、②③④ D、③④⑤
查看答案和解析>>
科目: 来源: 题型:
绿色化学的目标是 ( )
A.减少对环境的污染 B.防患于未然,最终杜绝化学污染源
C.设计对人类健康和环境更安全的化合物
D.研究变换基本原料和起始化合物
查看答案和解析>>
科目: 来源: 题型:
氨与硝酸在工农业生产中均有重要的用途。某小组根据工业生产原理设计了生产氨与硝酸的主要过程如下:
(1)以N2和H2为原料合成氨气。反应N2(g)+3H2(g)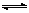 2NH3(g) △H<0
2NH3(g) △H<0
①一定温度下,在密闭容器中充入1molN2和3molH2发生反应。若容器容积恒定,达到平衡状态时,气体的总物质的量是原的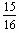 ,则N2的转化率α= ;若此时放出热量为aKJ,则其热化学方程式为 ___________________。
,则N2的转化率α= ;若此时放出热量为aKJ,则其热化学方程式为 ___________________。
②氨气溶于水则为氨水。已知NH3·H2O的电离平衡常数为Kb,计算0.1mol/L的NH3·H2O溶液中c(OH-)=___________mol/L(设平衡时NH3·H2O的浓度约为0.1mol/L,用含有Kb的代数式表示)。
(2)以氨气、空气为主要原料先进行氨的催化氧化,然后制得硝酸。
①其中NO在容积恒定的密闭容器中进行反应:
2NO(g)+O2(g)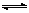 2NO2(g) △H>0
2NO2(g) △H>0
该反应的反应速率(v)随时间(t)变化的关系如下图所示。若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号) 。
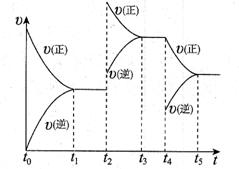
a.在t1~t2时,可依据容器内气体的密度保持不变判断反应已达到平衡状态
b.在t2时,采取的措施可以是升高温度
c.在t3~t4时与在t1~t2时的平衡常数K肯定相同
d.在t5时,容器内NO2的体积分数是整个过程中的最大值
②实际上,生成的NO2会聚合生成N2O4。如果在一密闭容器中,17℃、1.01×105Pa条件下,2NO2(g)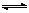 N2O4(g) △H<0的平衡常数K=13.3。若改变上述体系的某个条件,达到新的平衡后,测得混合气体中c(NO2)=0.04mol/L,c(N2O4)=0.007mol/L,则改变的条件是 。
N2O4(g) △H<0的平衡常数K=13.3。若改变上述体系的某个条件,达到新的平衡后,测得混合气体中c(NO2)=0.04mol/L,c(N2O4)=0.007mol/L,则改变的条件是 。
查看答案和解析>>
科目: 来源: 题型:
一定条件下,某容积为1L的密闭容器中发生如下反应:
C(s)+H2O(g) CO(g)+H2 (g)
CO(g)+H2 (g)
(1)维持温度不变,向该容器中充入2 mol C(s)和2 mol H2O(g),达到平衡后混合气体的平均相对分子质量为Mr,则Mr的范围为 。
(2)在(1)中若充入的是2.5 mol CO(g)和4 mol H2 (g),达到平衡后混合气体的平均相对分子质量为 ;若要求达到平衡后混合气体的平均相对分子质量始终大于该值,则充入的CO、H2混合气体的总质量m和总物质的量n必须满足的关系为
查看答案和解析>>
科目: 来源: 题型:
已知:CO(g)+H2O(g) CO2(g)+H2(g) △H= -42kJ·mol-1
CO2(g)+H2(g) △H= -42kJ·mol-1
(1)在一定温度下,向一定体积的密闭容器中通入1molCO、2molH2O(g),反应达平衡时,测得放出的热量为28kJ,求CO的转化率为 ;
(2)该温度下,向该密闭容器中通入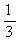 molCO2、
molCO2、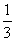 molH2,欲使反应达平衡时CO的体积分数与(1)相同,则还需满足的条件是 ;
molH2,欲使反应达平衡时CO的体积分数与(1)相同,则还需满足的条件是 ;
(3)该温度下,向该密闭容器中通入2molCO、3molH2O(g),反应达平衡时时,求H2O(g)的转化率 ;
(4)该温度下,向该密闭容器中通入1.5molCO、3molH2O(g),反应达平衡时,放出的热量为 kJ。
查看答案和解析>>
科目: 来源: 题型:
甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应制备甲醇。
Ⅰ:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206.0 kJ·mol-1
Ⅱ:CO(g)+2H2(g)===CH3OH(g) ΔH=-129.0 kJ·mol-1
(1)CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为_______________。
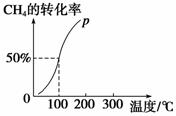 (2)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100 L的反应室中,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如右图。
(2)将1.0 mol CH4和2.0 mol H2O(g)通入容积为100 L的反应室中,在一定条件下发生反应Ⅰ,测得在一定的压强下CH4的转化率与温度的关系如右图。
①假设100 ℃时达到平衡所需的时间为5 min,则用H2表示该反应的平衡反应速率为____________________。
②100 ℃时反应Ⅰ的平衡常数为__________________。
(3)在压强为0.1 MPa、温度为300 ℃条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下发生反应Ⅱ生成甲醇,平衡后将容器的容积压缩到原的1/2,其他条件不变,对平衡体系产生的影响是________(填字母序号)。
A.c(H2)减小
B.正反应速率加快,逆反应速率减慢
C.CH3OH的物质的量增加
D.重新平衡c(H2)/c(CH3OH)减小
E.平衡常数K增大
查看答案和解析>>
科目: 来源: 题型:
将1.00 mol二氧化硫和1.00 mol氧气通入1.00 L的密闭容器中,分别在500 K,600 K,700 K三个不同的温度下进行2SO2+O2 2SO3反应,反应过程中SO3浓度随时间的变化如下面表格所示:
2SO3反应,反应过程中SO3浓度随时间的变化如下面表格所示:
表一:500 K
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| SO3浓度(mol·L-1) | 0 | 0.10 | 0.15 | 0.20 | 0.25 | 0.30 |
| 时间 | 30 | 35 | 40 | 45 | 50 | 55 |
| SO3浓度(mol·L-1) | 0.35 | 0.40 | 0.50 | 0.55 | 0.60 | 0.60 |
表二:600 K
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| SO3浓度(mol·L-1) | 0 | 0.20 | 0.30 | 0.40 | 0.50 | 0.50 |
表三:700 K
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| SO3浓度(mol·L-1) | 0 | 0.25 | 0.35 | 0.35 | 0.35 | 0.35 |
(1)从上面三个表的数据可以判断该反应是__________反应(填“吸热”或“放热”),利用表一计算0~40 min内用SO2表示该反应的化学反应速率v(SO2)=__________mol·L-1·min-1。
(2)对该反应,下面的说法正确的是__________。
A.当容器中的压强不再变化时,该反应就达到平衡
B.达到平衡时v正(SO2)=v逆(SO3)
C.平衡时c(SO2)=c(SO3)
D.当由500 K平衡状态时升高温度至600 K时,重新达到平衡状态时,容器的压强减小
(3)从上面三个表的数据,温度对该反应的反应速率和平衡移动的影响是_____________________________________________________________________。
(4)计算在600 K时的平衡常数(写出计算过程,最后结果取两位有效数字)。
(5)下图曲线(Ⅰ)是在500 K时SO3浓度的变化曲线,请你在图中画出在550 K进行上述反应的曲线,并标明曲线(Ⅱ)。
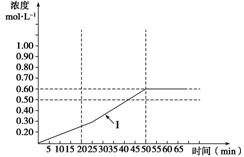
查看答案和解析>>
科目: 来源: 题型:
常温下,0.1 mol/L某一元酸(HA)溶液中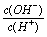 =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
A.溶液中水电离出的c(H+)=10-10 mol/L
B.溶液中c(H+)+c(A-)=0.1 mol/L
C.溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大
D.与0.05mol/L NaOH溶液等体积混合后所得溶液中离子浓度大小关系为
c(A-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目: 来源: 题型:
加热N2O5,依次发生的分解反应为①N2O5(g)  N2O3(g)+O2(g),②N2O3(g)
N2O3(g)+O2(g),②N2O3(g)  N2O(g)+O2(g)。在容积为2 L的密闭容器中充入8 mol N2O5,加热到t ℃,达到平衡状态后O2为9 mol,N2O3为3.4 mol,则t ℃时反应①的平衡常数为( )
N2O(g)+O2(g)。在容积为2 L的密闭容器中充入8 mol N2O5,加热到t ℃,达到平衡状态后O2为9 mol,N2O3为3.4 mol,则t ℃时反应①的平衡常数为( )
A.10.7 B.8.5 C.9.6 D.10.2
查看答案和解析>>
科目: 来源: 题型:
把3.0 mol M和2.5 mol N混合于2.0 L的恒容密闭容器中,发生反应3M(g)+N(g)  xP(g)+2Q(g),5 min反应达到平衡,已知M的转化率为50%,P的反应速率为0.15 mol·L-1·min-1,则下列说法正确的是
xP(g)+2Q(g),5 min反应达到平衡,已知M的转化率为50%,P的反应速率为0.15 mol·L-1·min-1,则下列说法正确的是
A.方程式中x=2
B.达平衡后,容器内压强是反应起始时的2倍
C.向容器中再充入3.0 mol M和2.5 mol N,达新平衡时Q的体积分数减小
D.容器内混合气体的密度不再变化和平均相对分子质量不再变化均可作为达到平 衡状态的标志
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com