
科目: 来源: 题型:
甲是一种盐,由A、B、C、D、E五种元素组成,其中四种是短周期元素。甲溶于水后可电离出由上述元素组成的三种离子,其中含有由A、B形成的10电子阳离子。A元素原子核内质子数比E的少1,D、E处于同主族。
用甲进行如下实验:
①取少量甲的晶体溶于蒸馏水配成溶液;
②取少量甲溶液于试管中加入适量NaOH溶液,加热;
③取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色;
④取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀。
回答下列问题:
(1)C在周期表中的位置 。
(2)实验②中出现的现象是 。
(3)用离子方程式表示实验③中现象的原因: ;若向此时溶液中加入KCl溶液,此溶液中的平衡(非水的电离平衡及盐的水解平衡)将 (填 “不移”,“左移”,“右移”)。
(4)由A、B、D、E组成的阳阴粒子个数比为1:2的盐X,在X的水溶液中,c(H+)==________________。
(5)经测定甲晶体的摩尔质量为392 g/mol,其中阳离子与阴离子物质的量之比为3:2,则甲晶体的化学式为 。
查看答案和解析>>
科目: 来源: 题型:
已知:乙二酸俗称草酸(结构简式为HOOC—COOH,可简写为H2C2O4)。
5℃时,草酸的电离平衡常数为K1=5.0×10-2,K2=5.4×10-5;
碳酸(H2CO3)的电离平衡常数为K1=4.5×10-7,K2= 4.7×10-11。
草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9。回答下列问题:
(1)写出水溶液中草酸的电离方程式 ;
(2)相同条件下等物质的量浓度的Na2C2O4溶液的pH比Na2CO3溶液的pH (填“大”、“小”或“相等”);
(3)常温下将0.4 mol/L的KOH溶液20 mL与0.2 mol/L的草酸溶液20 mL混合,则混合后溶液中阴离子浓度的大小顺序为__________________________;
(4)实验室常用酸性高锰酸钾溶液滴定草酸来测定草酸溶液的浓度。高锰酸钾溶常
用 (填“稀硫酸”、 “稀硝酸”、 “稀盐酸”)酸化,已知酸性高锰酸钾和草酸反应的现象是有气泡产生,紫色消失,其反应的离子方程式为 ;
(5)25℃时向20 mL碳酸钙的饱和溶液中逐滴加入8.0×10-4 mol/L的草酸钾溶液
20 mL,能否产生沉淀 (填“能”或“否”).
查看答案和解析>>
科目: 来源: 题型:
汽车作为一种现代交通工具正在进入千家万户,汽车尾气中含有CO、NOx等有毒气体,其污染问题也成为当今社会急需解决的问题。
(1)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图:
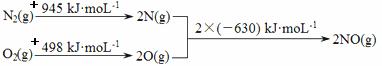
则该反应的热化学方程式为 。
(2)对汽车加装尾气净化装置,可使CO、NOx有毒气体相互反应转化为无毒气体。
2xCO+2NOx ==2xCO2+N2,当转移电子物质的量为0.6x mol时,该反应生成标准状况下N2 L。
(3)一氧化碳是一种用途相当广泛的化工基础原料。可以还原金属氧化物,还可以用来合成很多有机物如甲醇等。在压强为0.1 MPa条件下,将a mol CO与3a mol H2的混合气体在催化剂作用下反应生成甲醇: CO(g)+2H2(g)  CH3OH(g);△H= -bkJ•mol-1
CH3OH(g);△H= -bkJ•mol-1
①该反应的平衡常数表达式为 。
②若容器容积不变,下列措施可增加甲醇产率的是 。
A.升高温度 B.将CH3OH(g)从体系中分离
C.缩小体积,增大压强 D.再充入1 mol CO和3 mol H2
③经测定不同温度下该反应的平衡常数如下:
| 温度(℃) | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
若某时刻250℃测得该反应的反应物与生成物的浓度为c(CO) =0.8 mol/L、c(H2)=1.0mol/L、c(CH3OH)=0.8 mol·L-1, 则此时v正 v逆(填>、<或=)。
查看答案和解析>>
科目: 来源: 题型:
Li-SOCl2电池是一种新型电池。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 = 4LiCl +S +SO2。
(1)电池正极发生的电极反应为 ;
(2)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。 如果把少量水滴到SOCl2中,反应的化学方程式为 ;
(3)用Li-SOCl2电池在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜(含有少量的锌、铁、银、金等金属和少量矿物杂质)的提纯,并对阳极泥和电解液中金属进行回收和含量测定。请回答以下问题。
①电解时,电解过程中,硫酸铜的浓度会 选填“变大”“不变”或“变小”)。
②电解完成后,该小组同学将电解液过滤后对滤液和阳极泥分别进行处理:
阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式: .
③Cu的回收、滤液成分及含量的测定:以下是该小组设计的一个实验流程。
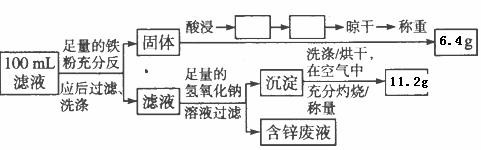
在上述流程中空格内填上相应的操作:过虑 、 ;100 mL滤液中 Fe2+的浓度为 mol/l
查看答案和解析>>
科目: 来源: 题型:
亚硝酸钠被称为工业盐,不能用作食品工业,但在漂白、电镀等方面应用广泛。现以木炭、浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如下图所示(部分夹持装置略)。
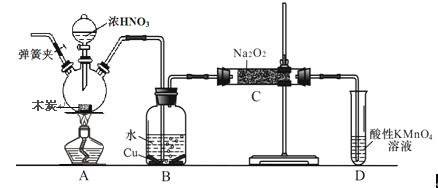

已知:①3NaNO2+3HCl == 3NaCl+HNO3+2NO↑+H2O②酸性条件下,NO或NO2– 都能与MnO4–反应生成NO3– 和Mn2+;
完成下列填空:
(1)写出a仪器的名称 。
(2)写出NO与过氧化钠在常温下转化成亚硝酸钠的化学反应方程式
(3) B中观察到的主要现象是有无色气体产生和 ,D装置中发生反应的离子方程式为 。
(4)检验C中产物有亚硝酸钠试剂是 。
(5)经检验C产物中除亚硝酸钠外还含有副产物碳酸钠和氢氧化钠,为避免产生这些副产物应在B、C装置间增加装置,则该装置中盛放的药品名称 。
(6)将7.8g过氧化钠完全转化成为亚硝酸钠,理论上至少需要木炭 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com