
科目: 来源: 题型:
2013年世界环境日中国主题为“同呼吸·共奋斗”,其中防治PM2.5是重点。PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是雾霾天气的主要原因,它主要来自化石燃料的燃烧,下列与PM2.5相关的说法不正确的是 ( )
A.大力发展电动车,减少燃油汽车的尾气排放量
B.开发利用各种新能源,减少对化石燃料的依赖
C.吸烟也会造成室内PM2.5污染
D.PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素
查看答案和解析>>
科目: 来源: 题型:
已知:反应Fe(s)+CO2(g)  FeO(s)+CO(g)的平衡常数为K1;
FeO(s)+CO(g)的平衡常数为K1;
反应Fe(s)+H2O(g)  FeO(s)+H2(g)的平衡常数为K2。不同温度时K1、K2的值如下表:
FeO(s)+H2(g)的平衡常数为K2。不同温度时K1、K2的值如下表:
| 温度/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
根据表中数据,计算反应CO2(g)+H2(g)  CO(g)+H2O(g)在973K时的平衡常数的K
CO(g)+H2O(g)在973K时的平衡常数的K
查看答案和解析>>
科目: 来源: 题型:
在400 ℃、101 kPa,将SO2和14 mol O2装入一个有催化剂的5 L密闭容器中,发生了2SO2(g)+O2(g)  2SO3(g)的反应,10 min时达到平衡时,测得容器内有2 mol SO2和12 mol O2 。则:(提示:用三步法)
2SO3(g)的反应,10 min时达到平衡时,测得容器内有2 mol SO2和12 mol O2 。则:(提示:用三步法)
(1)SO2的起始浓度
(2)平衡体系中含SO3的体积分数
查看答案和解析>>
科目: 来源: 题型:
如图为相互串联的甲、乙两电解池。
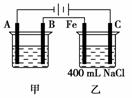
试回答:
(1)若甲池利用电解原理在铁上镀银,则A是________ (填电极材料),电极反应式是________________;应选用的电解质溶液是________。
(2)乙池中若滴入少量酚酞试液,开始电解一段时间,铁极附近呈________色
(3)若甲槽阴极增重43.2 g,则乙槽中阳极上放出的气体在标准状况下的体积是________mL。若乙槽中剩余溶液仍为400 mL,则电解后所得溶液的物质的量浓度为________ mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
由锌片、铜片和200 mL稀H2SO4组成的原电池如图所示。
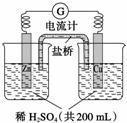
(1)原电池的负极反应式是_________________________________________________,
(2)电流的方向是_________________________________________________________。
(3)一段时间后,当在铜片上放出1.68 L(标准状况下)气体时,H2SO4恰好消耗一半。则产生这些气体的同时,共消耗________g锌
查看答案和解析>>
科目: 来源: 题型:
T ℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示。
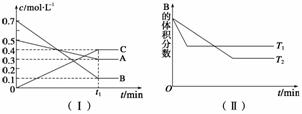
根据以上条件,回答下列问题:
(1) A与B反应生成C的化学方程式为________________________________________,
(2) 假如t1=5min,求用A表示t1这段时间内反应速率
(3) 正反应为________(填“吸热”或“放热”)反应。
(4)t1 min后,改变下列某一条件,能使平衡向逆反应方向移动的有(单选)__________
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量稀有气体
C.保持其他条件不变,升高温度
查看答案和解析>>
科目: 来源: 题型:
已知:①2C(s)+O2(g)===2CO(g) ΔH=-221.0 kJ·mol-1;
②2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1。
则制备水煤气的反应C(s)+H2O(g)===CO(g)+H2(g)的ΔH为(提示:运用盖斯定律)
查看答案和解析>>
科目: 来源: 题型:
(1)沼气是一种能源,它的主要成分是CH4。0.5 mol CH4完全燃烧生成CO2和液态H2O时,放出445 kJ热量,热化学方程式为______________________________________。
查看答案和解析>>
科目: 来源: 题型:
甲醇燃料电池(DMFC)可用于笔记本电脑、汽车、遥感通讯设备等,它的一极通入甲醇,一极通入氧气;电解质是质子交换膜,它能传导氢离子(H+)。电池工作时,甲醇被氧化为二氧化碳和水,氧气在电极上的反应是O2+4H++4e-===2H2O。下列叙述中不正确的是 ( )
A.负极的反应式为CH3OH+H2O-6e-===CO2↑+6H+
B.电池的反应方程式是2CH3OH+3O2===2CO2+4H2O
C.电池工作时,H+由正极移向负极
D.电池工作时,电子从通入甲醇的一极流出,经外电路再从通入氧气的一极流入
查看答案和解析>>
科目: 来源: 题型:
已知:2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1
H2(g)+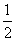 O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
由此可知,在等温下蒸发45 g液态水需吸收的热量( )
A.483.6 kJ B.110 kJ C.285.8 kJ D.221 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com