
科目: 来源: 题型:
下列说法正确的是
A.地沟油和矿物油都属于酯类物质
B.为测定熔融氢氧化钠的导电性,将氢氧化钠固体放在石英坩埚中加热熔化
C.在食品袋中放人盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质
D.电解从海水中得到的氯化镁溶液可获得金属镁
查看答案和解析>>
科目: 来源: 题型:
I、恒温下,将a mol N2与b mol H2的混合气体通入一个固体容积的密闭容器中,发生如下反应:N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,计算 a= 。
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量 。。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),
n( 始):n(平)= 。
(4)原混合气体中,a:b= 。
(5)达到平衡时,N2和H2的转化率之比,a(N2):a(H2)= 。
(6)平衡混合气体中,n(N2):n(H2):n(NH3)= 。
II、若向体积不变的密闭容器中充入2 mol N2和6 mol H2,一定条件下发生反应:
N2(g)+ 3 H2(g) 2 NH3(g),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(g),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
(1)若a=0,b=0,则c= .
(2)若a=0.7,b=2.1,则:
① c= .
②这时反应向 进行,因为: .
查看答案和解析>>
科目: 来源: 题型:
在体积为2 L的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
CO(g)+H2O(g) △H=Q,化学平衡常数K与温度T的关系如下表:
| T/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)Q____0(填 “>”、“<”),升高温度,化学平衡向________(填“正反应”或“逆反应”)方向移动。
(2)若某温度下,平衡浓度符合下列关系:c(CO2)·c(H2)=c(CO)·c(H2O),此时的温度为__________;在此温度下,若该容器中含有1mol CO2、3mol H2、2mol CO、2mol H2O,则此时反应所处的状态为____________(填“向正反应方向进行中”、“向逆反应方向进行中”或“平衡状态”),此温度平衡时CO2的浓度为___________ mol·L-1;在此温度下,若该容器中含有1.5mol CO2、3.5mol H2、1.5mol CO、1.5mol H2O达到平衡时CO2的浓度为___________ mol·L-1。
查看答案和解析>>
科目: 来源: 题型:
某温度时,在一个容积为2 L的密闭容器中,X、Y、Z,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
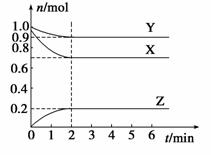
(1)该反应的化学方程式为_______________;
(2)反应开始至2 min,气体Z的反应速率为____________;
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________倍;
②若此时将容器的体积缩小为原来的 0.5倍,达到平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应的正反应为________反应(填“放热”或“吸热”)。
查看答案和解析>>
科目: 来源: 题型:
将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2  2SO3(正反应放热),反应达到平衡后,此时将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28 L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。
2SO3(正反应放热),反应达到平衡后,此时将容器中的混合气体通过过量NaOH溶液,气体体积减少了21.28 L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。
(1)求该反应达到平衡时SO2的转化率____ __(用百分数表示)。
(2)判断该反应达到平衡状态的标志是_______。(填字母)
a.SO2和SO3浓度相等 b.SO2百分含量保持不变
c.容器中气体的压强不变 d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(3)欲提高SO2的转化率,下列措施可行的是_______。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(4)若保持容积不变,当达到平衡时充入氩气,平衡将 (填“正向”“逆向”或“不移动”)。
(5)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将 (填“正向”“逆向”或“不”)移动。
查看答案和解析>>
科目: 来源: 题型:
一定条件下发生反应:
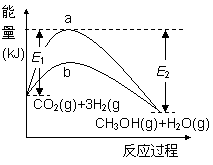
CO2(g)+3H2(g)  CH3OH(g)+H2O(g),右图表示该反应进行过程中的能量变化。
CH3OH(g)+H2O(g),右图表示该反应进行过程中的能量变化。
⑴图中曲线___(填“a”或“b”)表示使用催化剂时的反应进程。使用催化剂对该反应的影响是______(填选项字母)。
 A.提高反应速率
A.提高反应速率
B.提高CO2的转化率
C.降低反应活化能
D.改变反应的ΔH
 ⑵CO2(g)+3H2(g) CH3OH(g)+H2O(g)的化学平衡常数的表达式K=_______________________。升高温度,K值将_______(填“增大”、“减小”或“不变”)。
⑵CO2(g)+3H2(g) CH3OH(g)+H2O(g)的化学平衡常数的表达式K=_______________________。升高温度,K值将_______(填“增大”、“减小”或“不变”)。
⑶用含E1、E2的表达式表示
 CO2(g)+3H2(g) CH3OH(g)+H2O(g)的ΔH=______ kJ·mol-1
CO2(g)+3H2(g) CH3OH(g)+H2O(g)的ΔH=______ kJ·mol-1
⑷一定温度下,在体积为2L的容积固定的密闭容器中,充入2molCO2、6molH2,经10min反应达到平衡状态W,生成1molCH3OH。CO2的转化率为________。从反应开始到平衡,用H2的浓度变化表示的平均反应速率v(H2)=____________。该温度下,在体积为1L的容积固定的密闭容器中,从逆反应开始建立化学平衡,且各组分的平衡浓度与平衡状态W完全相同,则起始时充入容器的n(CH3OH)=________,n(H2O)=________。
查看答案和解析>>
科目: 来源: 题型:
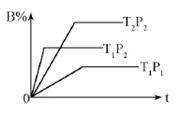
已知某可逆反应:mA(g)+nB(g)  pC(g) △H=Q kJ·mol-1 ,在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是
pC(g) △H=Q kJ·mol-1 ,在密闭容器中进行,下图表示在不同时间t、温度T、压强P与反应物B的百分含量的关系曲线,下列判断正确的是
A.T2 >T1 ? P1 > P2 m+n > p ?? Δ Η<0
B.T1 >T2 ? P1 < P2 m+n < p ? ? Δ Η>0
C.T1 <T2 ? P1 < P2 m+n < p ? ?Δ Η<0
D.T1 >T2 ? P1 < P2 m+n > p ?? Δ Η>0
查看答案和解析>>
科目: 来源: 题型:
在一定条件下发生反应:2A(g)+2B(g)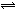 xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率VD=0.2mol/(L·min),下列说法正确的是:
xC(g)+2D(g),在2L密闭容器中,把4molA和2molB混合,2min后达到平衡时生成1.6molC,又测得反应速率VD=0.2mol/(L·min),下列说法正确的是:
A.A和B的转化率均是20%; B.x = 4;
C.平衡时A的物质的量为2.8mol; D.平衡时气体压强比原来减小。
查看答案和解析>>
科目: 来源: 题型:
关于下列装置说法正解的是( )
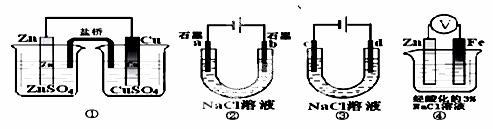
A.装置①中,盐桥中的Cl-移向CuSO4溶液
B.装置②工作一段时间后,a极附近溶液的pH降低
C.用装置③精炼铜时,c极为粗铜
D.装置④中电子由Zn流向Fe,Zn极发生氧化反应
查看答案和解析>>
科目: 来源: 题型:
在容积不变的密闭容器中存在如下反应:
2SO2(g)+O2(g) 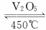 2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
2SO3(g) ΔH<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )

A.图Ⅰ表示的是t1时刻增大O2的浓度对反应速率的影响
B.图Ⅱ表示的是t1时刻加入催化剂后对反应速率的影响
C.图Ⅲ表示的是催化剂对平衡的影响,且甲的催化效率比乙高
D.图Ⅲ表示的是压强对化学平衡的影响,且乙的压强较高
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com