
科目: 来源: 题型:
下列卤代烃既能发生消去反应生成烯烃,又能发生水解反应生成醇的是
( )
①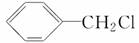 ②CH3CH2CH2Br ③CH3F
②CH3CH2CH2Br ③CH3F
④CH3CH2Br ⑤C(CH3)3CH2Br
⑥CH(CH3)2C(CH3)2Br
A.①③⑤ B.②④⑥
C.③④⑤ D.①②⑥
查看答案和解析>>
科目: 来源: 题型:
下列卤代烃在KOH醇溶液中加热不能发生消去反应的是
( )
①C6H5Cl ②(CH3)2CHCH2Cl ③(CH3)3CCH2Cl
④CHCl2—CHBr2 ⑤CH3CH2Br ⑥CH2Cl2
A.①③⑥ B.②③⑤
C.全部 D.②④
查看答案和解析>>
科目: 来源: 题型:
SO2是硫酸工业尾气的主要成分。实验室中,拟用如图所示流程,测定标准状况下体积为V L的硫酸工业尾气中SO2的含量。
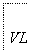
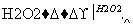

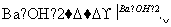
(1)步骤①中加入H2O2溶液时发生反应的离子方程式为____________________,1 mol H2O2参加反应,转移的电子数为________。
(2)步骤③的操作依次是过滤、________、________、称重。
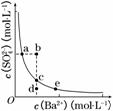
(3)一定温度下,BaSO4的沉淀溶解平衡曲线如图所示。步骤②逐滴加入Ba(OH)2溶液的过程中,BaSO4的溶度积常数________(填“增大”、“减小”或“不变”),溶液中SO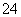 浓度的变化情况为________(填序号)。
浓度的变化情况为________(填序号)。
①d→c→e ②b→c→d ③a→c→e ④d→c→a
(4)该V L尾气中SO2的体积分数为________(用含有V、m的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
某化学课外兴趣小组为探究铜跟浓硫酸的反应情况,设计了下图所示装置进行有关实验:
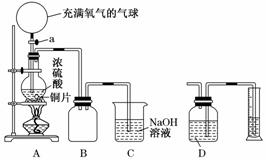
(1)先关闭活塞a,将6.4 g铜片和10 mL 18 mol/L的浓硫酸放在圆底烧瓶中共热至反应完成,发现烧瓶中还有铜片剩余。再打开活塞a,将气球中的氧气缓缓挤入圆底烧瓶,最后铜片完全消失。
①写出上述过程中圆底烧瓶内发生反应的化学方程式:
打开活塞a之前___________________________________________________;
打开活塞a之后___________________________________________________。
②B是用来收集实验中产生的气体的装置,但集气瓶内的导管未画全,请直接在图上把导管补充完整。
(2)实际上,在打开活塞a之前硫酸仍有剩余。为定量测定余酸的物质的量,甲、乙两学生进行了如下设计:
①甲学生设计的方案是:先测定铜与浓硫酸反应产生SO2的量,再通过计算确定余酸的物质的量。他测定SO2的方法是将装置A产生的气体缓缓通过装置D,从而测出装置A产生气体的体积(已折算成标准状况下)。你认为甲学生设计的实验方案中D装置中的试剂为______________________(填化学式)。
②乙学生设计的方案是:将反应后的溶液冷却后全部移入到烧杯中稀释,并按正确操作配制100 mL溶液,再取20 mL于锥形瓶中,用________作指示剂,用标准氢氧化钠溶液进行滴定[已知:Cu(OH)2开始沉淀的pH约为5],选择该指示剂的理由为__________________________________________________;再求出余酸的物质的量,若耗去a mol/L氢氧化钠溶液b mL,则原余酸的物质的量为________mol(用含a、b的表达式来表示)。
查看答案和解析>>
科目: 来源: 题型:
硅及其化合物对人类现代文明具有特殊贡献,请回答下列有关问题:
(1)硅原子的结构示意图:________。
(2)下列物品或设备所用的材料属于硅酸盐的是________。
①长江三峡水泥大坝 ②石英光导纤维 ③陶瓷坩埚 ④普通玻璃 ⑤硅太阳能电池
A.①②③ B.③④⑤
C.②③④ D.①③④
(3)常温下,SiCl4为液态,沸点为57.6℃,在空气中冒白雾。制备高纯度硅的中间产物SiCl4中溶有液态杂质,若要得到高纯度S iCl4,应采用的方法是________;用化学方程式及必要文字解释SiCl4在空气中冒白雾的原因:_______________________________________。
iCl4,应采用的方法是________;用化学方程式及必要文字解释SiCl4在空气中冒白雾的原因:_______________________________________。
(4)工业上可用SiCl4(g)制备高温结构陶瓷氮化硅,其反应方程式为
 3SiCl4(g)+2N2(g)+6H2(g)
3SiCl4(g)+2N2(g)+6H2(g)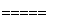 Si3N4(s)+12HCl(g) ΔH=a kJ/mol(a<0)
Si3N4(s)+12HCl(g) ΔH=a kJ/mol(a<0)
①该反应的平衡常数表达式K=______________.
②在密闭恒容容器中,能表示上述反应达到平衡状态的是_______ _。
_。
A.3v逆(N2)=v正(H2)
B.v正(HCl=4v正=4v正(SiCl4)
C.混合气体密度保持不变
D.c(N2)∶c(H2)∶c(HCl)=1∶3∶6
③在某条件下达到平衡时,H2与HCl物质的量之比为m∶n;保持其他条件不变,降低温度达到平衡时,H2与HCl物质的量之比________m∶n(填“>”、“=”或“<”)。
查看答案和解析>>
科目: 来源: 题型:
向一定量的Fe、FeO和Fe2O3的混合物中加入120 mL 4 mol·L-1的稀硝酸,恰好使混合物完全溶解,放出1.344 L NO(标准状况),往所得溶液中加入KSCN溶液,无红色出现。若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为( )
A.0.24 mol B.0.16 mol
C.0.21 mol D.0.14 mol
查看答案和解析>>
科目: 来源: 题型:
某混合气体X,可能由H2、CO、CO2和水蒸气中的一种或几种组成,现将混合气体通入灼热的CuO,完全反应后,固体CuO质量减少1.6 g;再将反应后的混合气体全部导入足量的澄清石灰水中,生成白色沉淀10 g。根据以上信息,分析下列有关X的组成推断正确的是( )
A.X一定只由CO组成
B.X一定只由H2和CO2组成
C.X可能由0.1 g H2和4.4 g CO2组成
D.X可能由0.1 g H2、1.4 g CO、2.2 g CO2组成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com