
科目: 来源:不详 题型:问答题
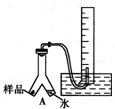
| 方案序号 | 所用试剂 | 净化剂 | 干燥剂 |
| A | MnO2、稀盐酸 | 饱和食盐水 | 浓硫酸 |
| B | Ca(ClO)2、浓盐酸 | 饱和食盐水 | 无水硫酸铜 |
| C | 氯酸钾、浓盐酸 | 饱和碳酸钠溶液 | 浓硫酸 |
| D | KMnO4、浓盐酸 | 水 | 碱石灰 |
查看答案和解析>>
科目: 来源: 题型:
 (烃基R中不含三键)。0.1molA与溶有96g液溴的四氯化碳恰好完全反
(烃基R中不含三键)。0.1molA与溶有96g液溴的四氯化碳恰好完全反查看答案和解析>>
科目: 来源:不详 题型:问答题
| H2SO4 |
| NaOH |
| NaOH |
| AlO | -2 |
| H2SO4 |
|
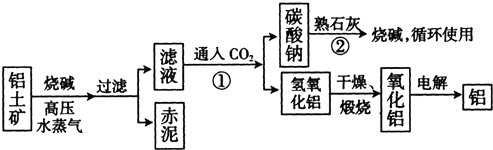
| Al2O3 | Fe2O3 | 其他杂质 | |
| 铝土矿 | 55% | 16% | - |
| 赤泥 | 15% | 48% | 一 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
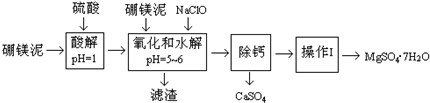
| 温度(°C) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.197 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.①②④③⑤ | B.②④①③⑤ | C.①③⑤②④ | D.④⑤③②① |
查看答案和解析>>
科目: 来源:长宁区一模 题型:多选题
| 操作 | 现象 | 结论 | |
| A | 向无水乙醇中加入浓H2SO4,加热至170℃产生的气体通入酸性KMnO4溶液 | 红色褪去 | 产生了乙烯 |
| B | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| C | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了NaHCO3 |
| D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A.A | B.B | C.C | D.D |
查看答案和解析>>
科目: 来源:潮州二模 题型:填空题
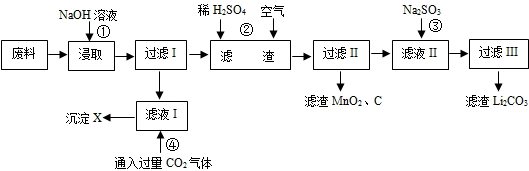
查看答案和解析>>
科目: 来源:广东模拟 题型:问答题
| 序号 | 反应物用量 | 产品质量 |
| 1 | n(H2SO4):n(Fe)>1:1 | 介于Ⅰ级~Ⅱ级之间 |
| 2 | n(H2SO4):n(Fe)<1:1 | 优于Ⅰ级 |
查看答案和解析>>
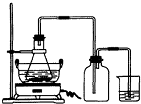
科目: 来源:上海 题型:问答题
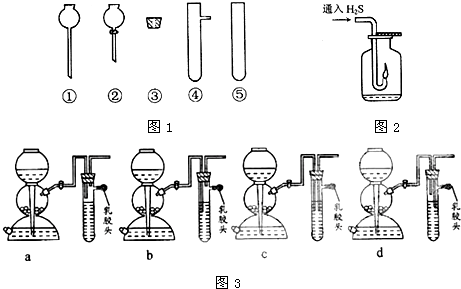
查看答案和解析>>
科目: 来源:诸城市模拟 题型:问答题
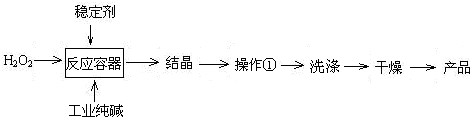
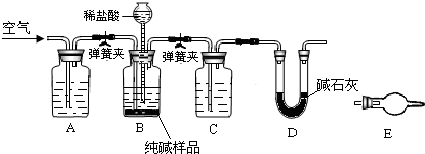
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com