
科目: 来源: 题型:
已知:I2+2S2O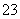 ===S4O
===S4O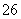 +2I-
+2I-
相关物质的溶度积常数见下表:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
(1)某酸性CuCl2溶液中含有少量的FeCl3,为得到纯净的CuCl2·2H2O晶体,加入____ ____,调至pH=4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中的c(Fe3+)=__ ______。过滤后,将所得滤液低温蒸发、浓缩结晶,可得CuCl2·2H2O晶体。
(2)在空气中直接加热CuCl2·2H2O晶体得不到纯的无水CuCl2,原因是(用化学方程式表示)_________________ ____________。由CuCl2·2H2O晶体得到纯的无水CuCl2的合理方法是_________ ___________________。
(3)某学习小组用“间接碘量法”测定含有CuCl2·2H2O晶体的试样(不含能与I-发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用0.100 0 mol·L-1 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。
①可选用______ __作滴定指示剂,滴定终点的现象是__________________ ____。
②CuCl2溶液与KI反应的离子方程式为__________ ________________。
③该试样中CuCl2·2H2O的质量百分数为____ ____。
查看答案和解析>>
科目: 来源: 题型:
羟基磷灰石是一种重要的生物无机材料,其常用的制备方法有两种:
方法A:用浓氨水分别调Ca(NO3)2和(NH4)2HPO4溶液的pH约为12;在剧烈搅拌下,将(NH4)2HPO4溶液缓慢滴入Ca(NO3)2溶液中。
方法B:在剧烈搅拌下,将H3PO4溶液缓慢滴加到Ca(OH)2悬浊液中。
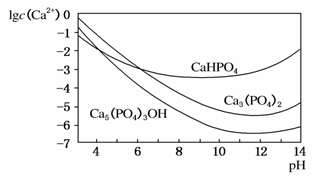
3种钙盐的溶解度随溶液pH的变化如图所示(图中纵坐标是钙离子浓度的对数),回答下列问题:
(1)完成方法A和方法B中制备Ca5(PO4)3OH的化学方程式:
①5Ca(NO3)2+3(NH4)2HPO4+4NH3·H2O===Ca5(PO4)3OH↓+____ _ ___+___ _____。
②5Ca(OH)2+3H3PO4===__________________ ____________。
(2)与方法A相比,方法B的优点是___________ ____________。
(3)方法B中,如果H3PO4溶液滴加过快,制得的产物不纯,其原因是_______________________________________________。
(4)图中所示3种钙盐在人体中最稳定的存在形式是________________(填化学式)。
查看答案和解析>>
科目: 来源: 题型:
现有电解质溶液:①Na2CO3 ②NaHCO3 ③NaAlO2 ④CH3COONa ⑤NaOH,且已知:CO2+3H2O+2AlO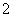 ===2Al(OH)3↓+CO
===2Al(OH)3↓+CO 。
。
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是__________________。
(2)将上述物质的量浓度均为0.1 mol·L-1的五种溶液,稀释相同倍数时,其pH变化最大的是______ __(填编号)。
(3)在上述五种电解质溶液中,分别加入AlCl3溶液,有气体产生的是____ ____(填编号)。
(4)将上述①②③④四种电解质溶液混合时,发生反应的离子方程式为____________________________________ _____________。
查看答案和解析>>
科目: 来源: 题型:
常温下,向20 mL氢氧化钠溶液中逐滴加入0.2 mol·L-1的CH3COOH溶液,滴定曲线如图所示:
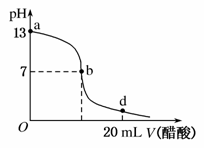
(1)该氢氧化钠溶液的物质的量浓度为______________。
(2)在b点,c(Na+)____ ____c(CH3COO-)(填“>”、“<”或“=”)。
(3)氢氧化钠溶液与CH3COOH溶液恰好完全反应的点位于曲线的____ ____(填选项的编号)。
A.a点 B.b点 C.d点 D.a、b间的某点 E.b、d间的某点
(4)在d点,溶液中所有离子的浓度由大到小的顺序为
____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
对于常温下的0.1 mol·L-1的NH4Cl溶液,请填空:
(1)溶液的pH________7(填“>”、“<”或“=”)。
(2)各类离子,其浓度由大到小的排列顺序是_________ _____。
(3)存在的电荷守恒关系为_____________ _______________。
(4)c(NH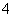 )+c(NH3·H2O)=____ ____(填数字或离子浓度均可)。
)+c(NH3·H2O)=____ ____(填数字或离子浓度均可)。
查看答案和解析>>
科目: 来源: 题型:
某温度时,测得0.01 mol·L-1的NaOH溶液的pH为11,则该温度下水的离子积常数为________________。
在此温度下将pH=a的H2SO4溶液VaL与pH=b的NaOH溶液VbL混合。
(1)若所得混合液为中性,且a=2,b=12,则Va:Vb=____ ____。
(2)若所得混合液的pH=10,且a=2,b=12,则Va:Vb=______ __。
查看答案和解析>>
科目: 来源: 题型:
一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示。已知:pM=-lg c(M),p(CO )=-lg c(CO
)=-lg c(CO )。下列说法正确的是 ( )
)。下列说法正确的是 ( )
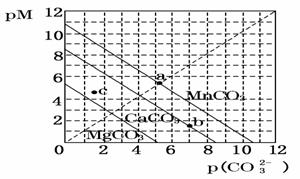
A.MgCO3、CaCO3、MnCO3的Ksp依次增大
B.a点可表示MnCO3的饱和溶液,且c(Mn2+) <c(CO )
)
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO )
)
D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)<c(CO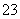 )
)
查看答案和解析>>
科目: 来源: 题型:
某温度下,相同pH值的盐酸和醋酸溶液分别加水稀释,平衡pH值随溶液体积变化的曲线如右图所示.据图判断正确的是( )
A.Ⅱ为盐酸稀释时的pH值变化曲线
B.b点溶液的导电性比c点溶液的导电性强
C.a点KW的数值比c点KW的数值大
D.b点酸的总浓度大于a点酸的总浓度
查看答案和解析>>
科目: 来源: 题型:
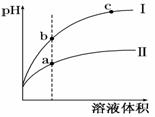
常温下,用0.100 0 mol·L-1 NaOH溶液滴定20.00 mL 0.100 0 mol·L-1 CH3COOH溶液,所得滴定曲线如图所示.下列说法正确的是( )
A.点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
B.点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-)
C.点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
D.滴定过程中可能出现:
c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
查看答案和解析>>
科目: 来源: 题型:
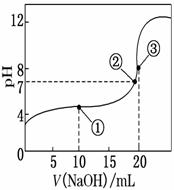
电离度是描述弱电解质电离程度的物理量,电离度=(已电离的物质的量/原来的总物质的量)×100%。现取20 mL pH=3的CH3COOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为( )
A.0.5% B.1.5% C.0.1% D.1%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com