
科目: 来源: 题型:
我国制碱工业的先驱——侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:NH3+C02+NaCl+H20→NH4CI+NaHCO3(晶体),依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。
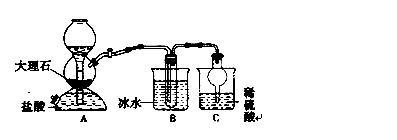
34.A装置中所发生反应的离子方程式为 C装置的作用为
35. 下表中所列出的是相关物质在不同温度下的溶解度数据(g/100 g水);

参照表中数据,请分析B装置中使用冰水的目的是 36.该校学生在检查完此套装置的气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用 。 37.若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85 g,实验后得到干燥的NaHCO3晶体的质量为5.04 g,则NaHCO3的产率为 。
查看答案和解析>>
科目: 来源: 题型:
研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) K1 Q > 0(I)
NaNO3(s)+ClNO(g) K1 Q > 0(I)
2NO(g)+Cl2(g) 2ClNO(g) K2 Q > 0 (II)
2ClNO(g) K2 Q > 0 (II)
28.由(I)(II)得到:4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)式子,请写出平衡常数表达式K= 。
2NaNO3(s)+2NO(g)+Cl2(g)式子,请写出平衡常数表达式K= 。
29.(2)为研究不同条件对反应(II)的影响,在恒温条件下,向 2L恒容密闭容器中加入0.2mol NO和0.1mol Cl2,10min时反应(II)达到平衡。测得10min内V(ClNO)=7.5×10-3mol?L-1?min-1,则平衡后n(Cl2)= mol,NO的转化率а1= 。30.其它条件保持不变,反应(II)在恒压条件下进行,平衡时NO的转化率а2 а1(填“>”“<”或“=”),平衡常数K2 (填“增大”“减小”或“不变”)。31.若要使K2减小,可采用的措施是 。
32.实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH→NaNO3+NaNO2+H2O。含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得 1L溶液A,溶液B为0.1mol?L?1的CH3COONa溶液,则两溶液中c(NO3?)、c(NO2?)和c(CH3COO?)由大到小的顺序为 。(已知HNO2的电离常数Ki=7.1×10-4mol?L?1,CH3COOH的电离常数K i=1.7×10-5mol?L?1)。
33.可使溶液A和溶液B的pH相等的方法是 。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d..向溶液B中加适量NaOH
查看答案和解析>>
科目: 来源: 题型:
部分中学化学常见元素原子结构及性质如表所示:
| 序号 | 元素 | 结构及性质 |
| A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 | |
| B | B原子最外层电子数是内层电子总数的1/5 | |
| ③ | C | C是常见化肥的主要元素,单质常温下呈气态 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ① | E | 通常情况下,E没有正化合价,A、B、C、D、F都能与E形成化合物 |
| ② | F | F在周期表中可以排在ⅠA族,也有人提出排在ⅦA族 |
23.A元素在周期表中的位置为____________________________________________。
24.B与C形成的化合物的化学式为________,它属于________(填“离子”或“共价”)化合物。
25.①F与E可以形成原子个数比分别为2∶1、1∶1的两种化合物X和Y,区别X与Y的水溶液的实验方法是___________________________________________________
________________________________________________________________________。
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则M的水溶液显________性,N的结构式为________。
26.C与E都是较活泼的非金属元素,用化学方程式表明这两种单质的氧化性强弱
________________________________________________________________________。
27.有人认为B、D的单质用导线连接后插入氯化钠溶液中可以形成原电池,你认为是否可以,若可以,试写出正极的电极方程式(若认为不行可不写)___________________
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
如图是一种综合处理SO2废气的工艺流程。若每步反应都完全,下列说法正确的是
(设反应过程中溶液的体积不变)( )
A.溶液B中发生的反应为:2SO2+O2→2SO3
B.由反应过程可推知氧化性:O2>Fe3+>SO42-
C.溶液的pH:A>B>C
D.A与C溶液成分相同,但浓度之比不同

查看答案和解析>>
科目: 来源: 题型:
部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
下列选项正确的是( )
A. 2CN-+H2O+CO2→2HCN+CO32-
B. 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
C. 物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-) < c(K+)-c(CN-)
D. c(NH4+) 相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中,
c(NH4HCO3)>c(NH4CN) >c(HCOONH4)
查看答案和解析>>
科目: 来源: 题型:
下列方程式正确的是( )
A.用铁丝网作电极,电解饱和食盐水:

B.Ba(OH)2溶液中加入过量的Al2(SO4)3溶液:
3Ba2++6OH-+2Al3++3SO →3BaSO4↓+2Al(OH)3↓
→3BaSO4↓+2Al(OH)3↓
C.向H218O中投入Na2O2固体: 2H218O + 2Na2O2→ 4Na+ + 4OH-+ 18O2↑
D.石灰乳中Ca(OH)2的电离:Ca(OH)2(s)  Ca2++ 2OH-
Ca2++ 2OH-
查看答案和解析>>
科目: 来源: 题型:
某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质.在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是( )

A.还原剂是含CN-的物质,氧化产物不只有N2
B.氧化剂是ClO-,还原产物是HCO3-
C.配平后氧化剂与还原剂的化学计量数之比为5:2
D.若生成2.24LN2则转移电子1mol
查看答案和解析>>
科目: 来源: 题型:
去甲肾上腺素可以调控动物机体的植物性神经功能,其结构简式如图所示。下列说法正确的是( )
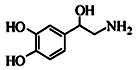
A.每个去甲肾上腺素分子中含有3个酚羟基
B.1mol去甲肾上腺素最多能与2molBr2
C.甲肾上腺素分子不能与饱和的碳酸氢钠溶液发生反应
D.去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应
查看答案和解析>>
科目: 来源: 题型:
向体积均为10 mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2得到溶液甲和乙;向甲、乙两溶液中分别滴加0.1mol·L-1盐酸,此时反应生成CO2体积(标准状况) 与所加盐酸体积间的关系如图所示。则下列叙述中正确的是( )
A.乙溶液中滴加盐酸后产生CO2体积的最大值为112mL(标准状况)
B.当0<V(HCl)<10mL时,甲溶液中发生反应的离子
方程式为: OH-+H+→H2O
C.乙溶液中含有的溶质是NaOH、NaHCO3
D. 原NaOH溶液的物质的量浓度为0.5 mol·L-1

查看答案和解析>>
科目: 来源: 题型:
已知氧化性Fe3+>I2。向Fe I 2溶液中通入一定量的Cl2,发生反应的离子方程式为: a Fe2++b I-+c Cl2→d Fe3++ e I2+ f Cl- 。下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是 ( )
A.2,4,3,2,2,6 B. 0,2,1,0,1,2
C.2,0,1,2,0,2 D. 2,8,5,2,4,10
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com