
科目: 来源: 题型:
下列叙述错误的是( )
|
| A. | 生铁中含有碳,抗腐蚀能力比纯铁弱 |
|
| B. | 用锡焊接的铁质器件,焊接处易生锈 |
|
| C. | 金属在海水中比在淡水中更易生锈 |
|
| D. | 电解熔融的氯化钠制取金属钠,用铁作阳极 |
查看答案和解析>>
科目: 来源: 题型:
我国某大城市今年夏季多次降下酸雨.据环保部门测定,该城市整个夏季酸雨的pH平均为3.2.在这种环境中的铁制品极易被腐蚀.对此条件下铁的腐蚀的叙述不正确的是( )
|
| A. | 此腐蚀过程有化学腐蚀也有电化学腐蚀 |
|
| B. | 发生电化学腐蚀时的正极反应为 2H2O+O2+4e﹣═4OH﹣ |
|
| C. | 在化学腐蚀过程中有氢气产生 |
|
| D. | 发生电化学腐蚀时的负极反应为Fe﹣2e﹣═Fe2+ |
查看答案和解析>>
科目: 来源: 题型:
关于如图所示装置的叙述,正确的是( )

A. 铜是阳极,铜片上有气泡产生
B. 盐桥中的阳离子会移向CuSO4溶液
C. 正极附近的SO42﹣离子浓度逐渐增大
D. 锌离子在锌片表面被还原
查看答案和解析>>
科目: 来源: 题型:
化学知识在生产、生活中有着广泛的应用.下列说法中不正确的是( )
A. 用植物秸秆、动物粪便等生产的沼气是一种清洁的能源
B. 手机上用的锂离子电池属于二次电池
C. 海水淡化能解决淡水供应危机,向海水中加净水剂明矾可以使海水淡化
D. 研制开发燃料电池汽车,可有效降低机动车尾气污染
查看答案和解析>>
科目: 来源: 题型:
工业上制备BaCl2的工艺流程图如下:
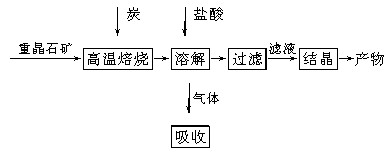
某研究小组在实验室用重晶石(主要成分为BaSO4)对工业过程进行模拟实验。查表得:
BaSO4(s)+4C(s)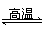
 4CO(g)+BaS(s)
4CO(g)+BaS(s)
ΔH1=571.2 kJ·mol-1 ①
BaSO4(s)+2C(s)
 2CO2(g)+BaS(s)
2CO2(g)+BaS(s)
ΔH2=226.2 kJ·mol-1 ②
(1)气体用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为________________________________________________________________________
________________________________________________________________________。
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,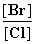 =__________________。
=__________________。
[Ksp(AgBr)=5.4×10-13 mol2·L-2,Ksp(AgCl)=2.0×10-10 mol2·L-2]
(3)反应:C(s)+CO2(g)
 2CO(g)的ΔH=________kJ·mol-1。
2CO(g)的ΔH=________kJ·mol-1。
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是
________________________________________________________________________,
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
温度t℃时,某NaOH稀溶液中[H+]=10-a mol·L-1,[OH-]=10-b mol·L-1,已知a+b=12,请回答下列问题:
(1)该温度下水的离子积常数KW=
________________________________________________________________________。
(2)该NaOH溶液中NaOH的物质的量浓度为
________________________________________________________________________,
该NaOH溶液中由水电离出的[OH-]为__________。
(3)给该NaOH溶液加热,pH________(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
一定温度下有:a.盐酸 b.硫酸 c.醋酸三种酸。
(1)当其物质的量浓度相同时,[H+]由大到小的顺序是______________。
(2)同体积、同物质的量浓度的三种酸,中和NaOH能力的顺序是____________。
(3)当其[H+]相同时,物质的量浓度由大到小的顺序为______________。
(4)当其[H+]相同、体积相同时,分别加入足量锌,相同状况下产生气体的体积由大到小的顺序为_________________________________________________________________。
(5)当[H+]相同、体积相同时,同时加入锌,若产生相同体积的H2(相同状况),则开始时的反应速率________,反应所需时间__________。
(6)将[H+]相同的三种酸均稀释10倍后,[H+]由大到小的顺序是______________。
查看答案和解析>>
科目: 来源: 题型:
某二元酸(化学式用H2A表示)在水溶液中的电离方程式是H2A===H++HA-;HA-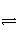

H++A2-。
回答下列问题:
(1)Na2A溶液显________(填“酸性”、“中性”或“碱性”),理由是(用离子方程式表示)________________________________________________________________________。
(2)若0.1 mol·L-1 NaHA溶液的pH=2,则0.1 mol·L-1 H2A溶液中氢离子的物质的量浓度可能__________0.11 mol·L-1(填“>”、“=”或“<”),理由是
________________________________________________________________________
__________________。
(3)0.1 mol·L-1 NaHA的溶液中各种离子浓度由大到小的顺序是
________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是( )
A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO 和OH-
和OH-
B.NaHCO3溶液中:[H+]+[H2CO3]=[OH-]
C.10 mL 0.10 mol·L-1 CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:[Na+]>[CH3COO-]>[OH-]>[H+]
D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com