
科目: 来源: 题型:
在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g)+2Y(g) 2Z(g),此反应达到平衡的标志是( )
2Z(g),此反应达到平衡的标志是( )
A.容器内压强不随时间变化 B.υ正(X)=υ逆(Z)
C.容器内X、Y、Z的浓度之比为l:2:2 D.单位时间消耗0.1molX同时生成0.2molZ
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式中,属于水解反应的是( )
A.CH3COOH+H2O CH3COO--+H3O+ B.CO2+H2O
CH3COO--+H3O+ B.CO2+H2O HCO3--+H+
HCO3--+H+
C.CO32--+H2O HCO3--+OH-- D.HS--+H2O
HCO3--+OH-- D.HS--+H2O S2--+H3O+
S2--+H3O+
查看答案和解析>>
科目: 来源: 题型:
已知汽车尾气无害化处理反应为:2NO(g)+2CO(g) N2(g)+2CO2(g)。下列说法不正确的是( )
N2(g)+2CO2(g)。下列说法不正确的是( )
A.升高温度可使该反应的逆反应速率降低
B.使用高效催化剂可有效提高该反应的速率
C.反应达到平衡后,NO的反应速率保持恒定
D.单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡
查看答案和解析>>
科目: 来源: 题型:
化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.铝盐(明矾溶液)和铁盐(硫酸铁溶液)都有净水作用,两者的作用原理是相同的
B.放在冰箱中的食品保质期较长,这与温度对反应速率的影响有关
C.0.1mol/L的CH3COONa溶液的pH约为9,说明CH3COOH是弱酸
D.室温下向10mLpH=3的醋酸溶液中加入水稀释后,溶液中导电粒子的数目减少
查看答案和解析>>
科目: 来源: 题型:
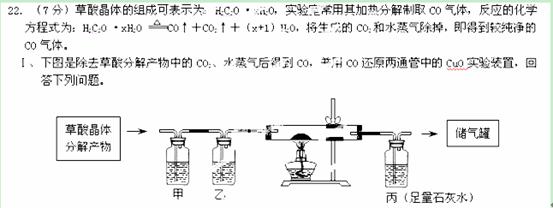
(1)在甲洗气瓶中所盛溶液是 ▲ 。
(2)CuO全部被还原后停止实验操作的步骤的有:①停止通气体,②熄灭酒精灯,③拆下实验装置, ④继续通气体到两通管冷却止。其正确的操作顺序是 ▲ 。
A.④②①③ B.①②③ C.②④①③ D.②④③
Ⅱ、为测定草酸晶体的x值,进行下列实验:
①取wg草酸晶体配成100mL水溶液;
②量取25.00mL草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol·L-1KMnO4溶液滴定。滴定时,所发生的反应为:
2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O
请回答下列问题:
(1)实验②中,滴定时,KMnO4溶液应装在 ▲ (填“酸式滴定管”、“碱式滴定管”)中。
(2)判断滴定终点的方法是 ▲ 。若滴定时,前后两次读数分别为a mL和b mL,由此计算出该草酸晶体的x值是 ▲ 。
(3)下列操作会引起测得的x值偏大的是 ▲ (填选项)
A.滴定结束时俯视读数
B.滴定结束后滴定管尖嘴处还有一滴标准液悬而未滴
C.锥形瓶未干燥即装入草酸溶液
D.滴定管用蒸馏水洗净后即装入KMnO4溶液
查看答案和解析>>
科目: 来源: 题型:
某研究性学习小组在研究二氧化硫漂白作用时,从“氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白作用”得到启发。为了探究二氧化硫作用得到底是二氧化硫本身还是二氧化硫与水作用的产物,该小组设计了如下实验。请回答相关问题。
(1)实验室用亚硫酸钠粉末跟硫酸制取二氧化硫,现有下列三种硫酸溶液,应选用 ▲ (填字母)。
A.98%浓硫酸 B.70%硫酸 C.10%稀硫酸
(2)为了探究SO2能否使品红褪色,该同学选择了正确的药品后设计了如下图所示实验装置,请指出实验装置设计中的不合理之处。
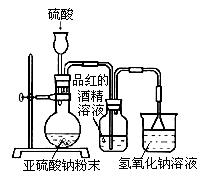
① ▲ ;② ▲ 。
(3)该同学选择了正确装置后,实验中控制二氧化硫以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色。为此,你认为使品红的水溶液褪色的微粒可能是 ▲ 。
(4)该同学进一步实验如下:取等量相同浓度的品红水溶液于两支试管中,再分别加入少量亚硫酸钠固体和亚硫酸氢钠固体,两支试管中的品红都褪色,他得出的结论:使品红褪色的微粒肯定是HSO3-或SO32-。你认为他的结论是否正确 ▲ ,其理由是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
溴化钙可用作阻燃剂、制冷剂,具有易溶于水,易吸潮等性质。实验室用工业大理石(含有少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下:

完成下列填空:
(1)上述使用的氢溴酸的质量分数为26%,若用47%的氢溴酸配置26%的氢溴酸的HBr
500ml,所需的玻璃仪器有玻璃棒、烧杯、量筒、 ▲ 、 ▲ 。
(2)已知步骤Ⅲ的滤液中不含NH4+。步骤Ⅱ加入的试剂a是 ▲ ,控制溶液的pH
约为8.0的目的是 ▲ 。步骤Ⅳ的目的是 ▲ 。
(3)制得的溴化钙可以通过如下步骤测定其纯度:
①称取4.00g无水溴化钙样品;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤、洗涤、
干燥、称量。若得到1.88g碳酸钙,则溴化钙的质量分数为 ▲ (保留两位小数)。
②若实验操作规范而测定结果偏低,其原因是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,
用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:

(1)相同条件下,相等物质的量浓度的
NH4Al(SO4)2中c(NH4+) ▲ (填“=”、“>” “<”)NH4HSO4中c(NH4+)。
(2)如图1是0.1mol•L﹣1电解质溶液的pH随温度变化的图象。
①其中符合0.1mol•L﹣1 NH4Al(SO4)2的pH随温度变化的曲线是 ▲ (填写字母);
②室温时时,0.1mol•L﹣1 NH4Al(SO4)2中
2c(SO42﹣)﹣c(NH4+)﹣3c(Al3+)= ▲ mol•L﹣1(填数值)
(3)室温时,向100mL 0.1mol•L﹣1 NH4HSO4溶液中滴加0.1mol•L﹣1 NaOH溶液,得到的溶液
pH与NaOH溶液体积的关系曲线如图2所示。
试分析图中a、b、c、d四个点,水的电离程度最大的是 ▲ ;在b点,溶液中各离子浓度由大到小的排列顺序是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
 (1)据报道以硼氢化合物NaBH4(H的化合价为-1价)和H2O2作原料的燃料电池,可用作通信卫星电。负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。写出该电池放电时负极的电极反应式:
(1)据报道以硼氢化合物NaBH4(H的化合价为-1价)和H2O2作原料的燃料电池,可用作通信卫星电。负极材料采用Pt/C,正极材料采用MnO2,其工作原理如图所示。写出该电池放电时负极的电极反应式:
▲ 。
(2)火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢
为助燃剂。
已知: N2H4(l) + O2(g) = N2(g)+ 2H2O(l) △H = – 534 kJ·mol—1
H2O2(l)= H2O(l) + 1/2O2(g) △H = – 98.6 kJ·mol—1
写出常温下,N2H4(l) 与 H2O2(l)反应生成N2和H2O的热化学方程式 ▲ 。
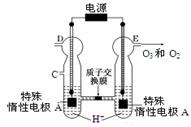 (3)O3可由臭氧发生器(原理如右图所示)电解稀硫酸制得。
(3)O3可由臭氧发生器(原理如右图所示)电解稀硫酸制得。
①图中阴极为 ▲ (填“A”或“B”)。
②若C处通入O 2,则A极的电极反应式为: ▲
(4)向一密闭容器中充入一定量一氧化碳跟水蒸气发生反应 CO(g)+H2O(g) CO2(g)+H2(g),下列情况下能判断该反应一定达到平衡状态的是____ ▲ _____(选填编号)。
CO2(g)+H2(g),下列情况下能判断该反应一定达到平衡状态的是____ ▲ _____(选填编号)。
A.v正(H2O) = v逆(H2)
B.容器中气体的压强不再发生改变
C.H2O的体积分数不再改变
D.容器中CO2和H2的物质的量之比不再发生改变
E.容器中气体的密度不再发生改变
 (5)温度T1时,在一体积为2L的密闭容积中,加入0.4molCO2和0.4mol的H2,反应中c(H2O)的变化情况如图所示,T1时反应CO(g)+H2O(g)
(5)温度T1时,在一体积为2L的密闭容积中,加入0.4molCO2和0.4mol的H2,反应中c(H2O)的变化情况如图所示,T1时反应CO(g)+H2O(g) CO2(g)+H2(g)第4分钟达到平衡。在第5分钟时向体系中同时再充入0.1molCO和0.1molH2(其他条件不变),请在右图中画出第5分钟到9分钟c(H2O)浓度变化趋势的曲线。
CO2(g)+H2(g)第4分钟达到平衡。在第5分钟时向体系中同时再充入0.1molCO和0.1molH2(其他条件不变),请在右图中画出第5分钟到9分钟c(H2O)浓度变化趋势的曲线。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com