
科目: 来源: 题型:
在80 g密度为d g·cm-3的硫酸铁溶液中,含有2.8 g Fe3+,则此溶液中SO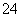 的物质的量浓度为(单位为mol·L-1)
的物质的量浓度为(单位为mol·L-1)
A.15d/16 B.5d/16 C.3d/8 D.5d/8
查看答案和解析>>
科目: 来源: 题型:
已知:还原性强弱:I— >Fe2+。往100 mL碘化亚铁
溶液中缓慢通入3.36 L(标准状况)氯气,反应完成后溶液中有1/2的Fe2+被氧化成Fe3+。则原碘化亚铁溶液的物质的量浓度为
A.1.1mol·L-1 B.1.5mol·L-1 C.1.2mol·L-1 D.1.0mol·L-1
查看答案和解析>>
科目: 来源: 题型:
现有等物质的量的铜和银的混合物17.2 g,与50.0 mL
的浓硝酸恰好完全反应,
产生气体4.48 L(标准状况),则下列说法正确的是
A.产生的气体是0.2 mol NO2
B.硝酸的物质的量浓度为12 mol·L-1
C.反应中被还原和未被还原的硝酸物质的量之比为3∶2
D.要使产生的气体恰好完全被水吸收需要通入氧气0.075 mol
查看答案和解析>>
科目: 来源: 题型:
ClO2气体是一种常用的消毒剂,我国从2 000年起逐步用ClO2代替氯气对饮用水进行消毒。
(1)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,在这个过程中,Fe2+、Mn2+的化合价升高,说明ClO2具有____▲__性。
(2)工业上可以通过下列方法制取ClO2,请完成该化学反应方程式:
2KClO3+SO2===2ClO2+______▲____。
(3)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8 mg·L-1之间。碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O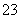 +I2===S4O
+I2===S4O +2I-)
+2I-)
Ⅲ.加硫酸调节水样pH至1~3。
操作时,不同pH环境中粒子种类如下图所示:
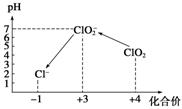
请回答:
①操作Ⅰ中反应的离子方程式是_____________▲_________________。
②确定操作Ⅱ完全反应的现象是_____________▲_________________。
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是_______▲___________。
④若水样的体积为1.0 L,在操作Ⅱ时消耗了1.0×10-3 mol·L-1的Na2S2O3溶液10 mL,则水样中ClO2的浓度是____▲____mg·L-1。
查看答案和解析>>
科目: 来源: 题型:
两种大气污染物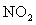 和
和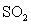 在一定条件下可发生如下反
在一定条件下可发生如下反
应:NO2 + SO2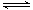 NO + SO3,在体积为VL的密闭容器中通入
NO + SO3,在体积为VL的密闭容器中通入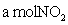 和
和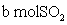 ,反应后容器内硫原子和氧原子的个数比为( )
,反应后容器内硫原子和氧原子的个数比为( )
A.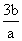 B.
B.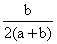 C.
C.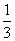 D.
D.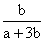
查看答案和解析>>
科目: 来源: 题型:
1.92gCu片与一定量的浓HNO3作用,当收集到NO2和
NO气体共1.12L时(标准状况),
金属铜恰好全部作用。则:
(1)反应中消耗HNO3 mol,转移电子 mol
(2)用排水法收集生成的气体,最后气体的体积为 L (标准状况)
(3)向收集到的气体中通入 mL O2(标准状况)才能使水刚好充满整个集气容器。
查看答案和解析>>
科目: 来源: 题型:
实验室需用2 mol·L-1氯化钠溶液450 mL,配置时应选用
容量瓶的规格和称取氯化钠的质量分别是
A. 450 mL,52.7g B.500 mL,58.5g C.1000 mL,117g D.任意规格,111.2g
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏伽德罗常数。下列叙述正确的是 ( )
A.1mol甲醇中含有C-H键的数目为4NA
B.标准状况下,2.24L已烷含有分子的数目为0.1NA
C.12克金刚石中含有的共价键数目为2NA
D.1 mol 甲基所含的电子数为10NA
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数,下列叙述正确的是(Fe 56)
A.1mol•L-1 NaHCO3溶液中的Na+数为NA
B.常温时,2.24LCO2所含的氧原子数为0.2NA
C.5.6g Fe与足量稀盐酸反应,转移电子数为0.2NA
D.标准状况下,2.24L CCl4所含分子数为0.1NA
查看答案和解析>>
科目: 来源: 题型:
1.52g铜镁合金完全溶解于50mL密
度为1.40g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120mL(标准状况),向反应后的溶液中加入1.0mol·L-1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀。
(1)该合金中铜与镁的物质的量之比是 。
(2)NO2和N2O4的混合气体中,NO2的体积分数是 。
(3)得到2.54 g沉淀时,加入NaOH溶液的体积是 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com