
科目: 来源:模拟题 题型:实验题
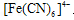 反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高。结合新信息,请你设计以下实验验证猜想:
反应生成蓝色沉淀,用K4[Fe(CN)6]溶液检验Fe3+的灵敏度比用KSCN更高。结合新信息,请你设计以下实验验证猜想: 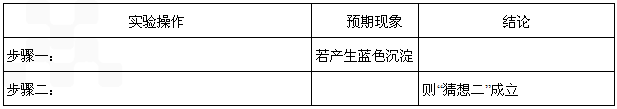
查看答案和解析>>
科目: 来源:模拟题 题型:实验题
查看答案和解析>>
科目: 来源:模拟题 题型:实验题




查看答案和解析>>
科目: 来源:期末题 题型:实验题
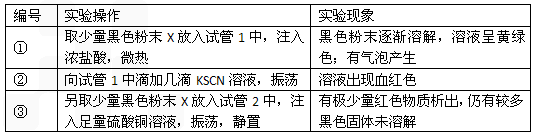
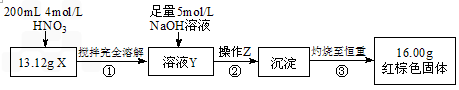
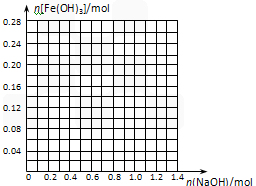
查看答案和解析>>
科目: 来源:期末题 题型:实验题
 3Cu+N2+3H2O
3Cu+N2+3H2O  Cu+Cu2+ 。
Cu+Cu2+ 。 
查看答案和解析>>
科目: 来源:同步题 题型:实验题

查看答案和解析>>
科目: 来源:同步题 题型:实验题
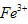 外还可能含有
外还可能含有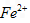 。若要确认其中的
。若要确认其中的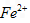 ,应选用_____________。
,应选用_____________。 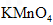 溶液
溶液 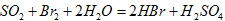
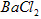 溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中
溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中 的体积分数为____________。
的体积分数为____________。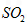 体积分数的结果,丙同学认为气体Y中还可能含量有
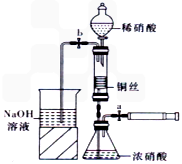
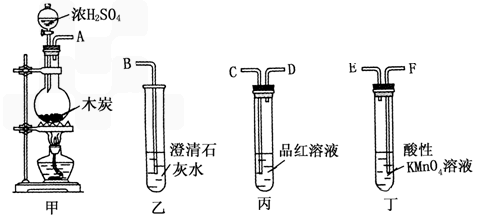
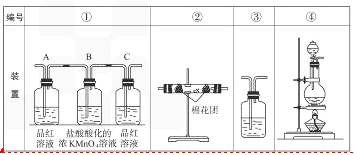
体积分数的结果,丙同学认为气体Y中还可能含量有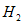 和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。
和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。 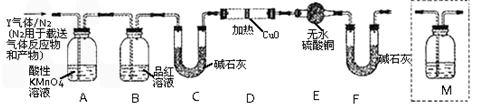
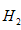 ,预计实验现象应是______________。
,预计实验现象应是______________。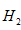 的含量(标准状况下约有
的含量(标准状况下约有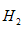 28ml ),除可用测量
28ml ),除可用测量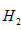 体积的方法外,可否选用质量称量的方法?做出判断并说明理由____________________.
体积的方法外,可否选用质量称量的方法?做出判断并说明理由____________________.查看答案和解析>>
科目: 来源:同步题 题型:实验题
查看答案和解析>>
科目: 来源:同步题 题型:实验题

查看答案和解析>>
科目: 来源:同步题 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com