
科目: 来源: 题型:
用NA表示阿伏加德罗常数,下列叙述正确的是( )
A.46 g乙醇中含有的化学键数为7NA
B.1 mol氯气和足量NaOH溶液反应转移电子数为2NA
C.1 mol OH-和1 mol —OH(羟基)中含有的质子数均为9NA
D.10 L 0.1 mol·L-1的Na2CO3溶液中,Na+、CO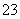 总数为3NA
总数为3NA
查看答案和解析>>
科目: 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
B.78 g苯含有C===C键的数目为3 NA
C.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA
查看答案和解析>>
科目: 来源: 题型:
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,8 g O2含有4nA个电子
B.1 L 0.1 mol·L-1的氨水中有nA个NH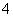
C.标准状况下,22.4 L盐酸含有nA个HCl分子
D.1 mol Na被完全氧化生成Na2O2,失去2nA个电子
查看答案和解析>>
科目: 来源: 题型:
某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数,下列说法中正确的是( )
①氯元素的相对原子质量一定是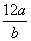 ②m g该氯原子的物质的量一定是
②m g该氯原子的物质的量一定是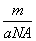 mol ③该氯原子的摩尔质量是aNA g/mol ④a g该氯原子所含质子数是17 mol
mol ③该氯原子的摩尔质量是aNA g/mol ④a g该氯原子所含质子数是17 mol
A.①③ B.②④
C.①④ D.②③
查看答案和解析>>
科目: 来源: 题型:
只给出下列甲和乙中对应的物理量,不能求出物质的量的是( )
A.甲:物质中的粒子数;乙:阿伏加德罗常数
B.甲:标准状况下的气体摩尔体积;乙:标准状况下的气体体积
C.甲:固体的体积;乙:固体的密度
D.甲:溶液中溶质的物质的量浓度;乙:溶液体积
查看答案和解析>>
科目: 来源: 题型:
下表是元素周期表的一部分。
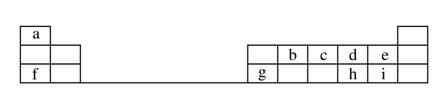
回答下列问题:
(1)元素b在元素周期表中的位置是________。
(2)元素a与c形成的4核10电子分子的化学式为________,其水溶液呈________性。
(3)元素e的负一价离子的结构示意图为________,元素g的简单离子的结构示意图为________,二者的离子半径大小顺序为________。
(4)元素i的气态氢化物比元素e的气态氢化物________(填“稳定”或“不稳定”)。
(5)元素i的单质溶于元素f的最高价氧化物对应的水化物中,可生成具有漂白作用的一种盐,该盐的电子式为______________,该化合物中所含的化学键类型为________________。
(6)元素d与h形成的化合物的化学式为____________________。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D为四种短周期元素,原子序数依次增大,原子半径按C、D、B、A的顺序逐渐减小。A、C位于同一主族,B、D位于同一主族;A、C的原子核内质子数之和为B、D的原子核内质子数之和的一半;C元素与其他三种元素均能形成离子化合物。
试回答下列问题:
(1)B的离子符号为________;C、D形成的化合物的电子式为________。
(2)同时含有上述四种元素的化合物有多种,写出其中任意一种化合物的化学式__________________________________________。
(3)由A、B、C中的两种元素组成的两种化合物相互反应生成A单质的化学方程式为__________________________________。
(4)由B、C、D中的两种元素组成的两种化合物发生的反应既属于化合反应又属于氧化还原反应,该反应的化学方程式为______。
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D是元素周期表中的四种短周期元素。
| 元素 | 性质或结构信息 |
| A | 单质制成的高压灯,发出的黄光透雾力强、射程远、且其单质燃烧后生成淡黄色固体 |
| B | 工业上通过分离液态空气获得其单质。原子的最外层电子数是其内层电子总数的2.5倍 |
| C | 单质是双原子分子,常温、常压下是淡黄绿色气体,原子的L层再增加1个电子即达到8电子稳定结构 |
| D | +2价阳离子的核外电子排布与氖原子相同 |
请根据表中信息回答下列问题:
(1)表中与元素A属于同一周期的元素是________(填字母),写出其离子的结构示意图________。
(2)已知C单质能与H2O发生置换反应生成O2,写出C单质与水反应的化学方程式__________________。
(3)对元素B的单质或化合物描述正确的是________。
a.元素B的最高正化合价为+6
b.常温常压下,其单质难溶于水
c.单质分子中含有18个电子
d.在一定条件下,氢气能与B单质反应
(4)A和D两种元素中活动性较强的是________(填元素符号),判断依据是________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
用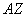 X表示原子:
X表示原子:
(1)中性原子的中子数:N=________。
(2)阳离子的中子数:AXn+共有x个电子,则N=________。
(3)阴离子的中子数:AXn-共有x个电子,则N=________。
(4)中性分子中子数:12C18O2分子中,N=________。
(5)A2-原子核内有x个中子,其质量数为m,则n gA2-所含电子的物质的量为________mol。
(6)某元素的同位素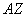 X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:
X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:
①Z值和A值:Z=________,A=________;
②X元素在周期表中的位置_____________________________。
查看答案和解析>>
科目: 来源: 题型:
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第ⅤA族,甲和丙位于同一主族,丁原子的最外层电子数与电子层数相等。下列判断正确的是( )
A.原子半径:丙>乙>丁
B.单质的还原性:丁>丙>甲
C.甲、乙、丙的氧化物均为共价化合物
D.乙、丙、丁的最高价氧化物对应的水化物能相互反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com