
科目: 来源:同步题 题型:实验题
查看答案和解析>>
科目: 来源:同步题 题型:实验题

查看答案和解析>>
科目: 来源:同步题 题型:实验题

 mMn+(aq)+nAm-(aq)
mMn+(aq)+nAm-(aq) 性,查得如下资料:(25 ℃)
性,查得如下资料:(25 ℃)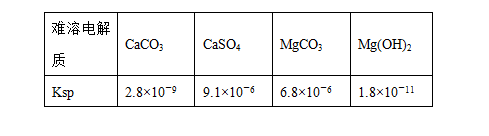
 液中加入固体Na2CO3 3 g,搅拌,静置,沉淀后弃去上层清液。
液中加入固体Na2CO3 3 g,搅拌,静置,沉淀后弃去上层清液。查看答案和解析>>
科目: 来源:江西省模拟题 题型:实验题
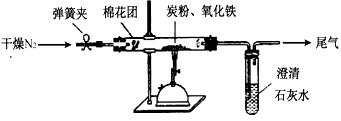
(2)查阅资料
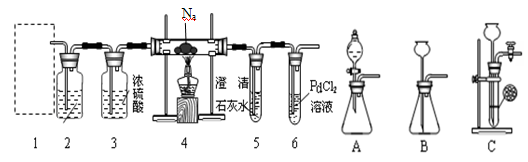
氮气不与碳、氧化铁发生反应。实验室可以用氯化铵饱和溶液和亚硝酸钠(NaNO2)饱和溶液混合加热反应制得氮气。
①请写出该反应的离子方程式____________________。
②该实验装置与实验室制取下列气体相同的是________(填标号);
A、用稀盐酸和锌反应制H2
B、用MnO2和浓盐酸加热反应制Cl2
C、用KClO3与MnO2共热反应制O2
(3)实验步骤
① 按上图连接装置,并检查装置的气密性,称取3.20g氧化铁、2.00g碳粉混合均匀,放入48.48g的硬质玻璃管中;
②加热前,先通一段时间纯净干燥的氮气;
③停止通入N2后,夹紧弹簧夹,加热一段时间,澄清石灰水(足量)变浑浊;
④待反应结束,再缓缓通入一段时间的氮气。冷却至室温,称得硬质玻璃管和固体总质量为52.24g;
⑤过滤出石灰水中的沉淀,洗涤、烘干后称得质量为2.00g。
步骤②、④中都分别通入N2,其作用分别为________。
(4)数据处理试根据实验数据分析,写出该实验中氧化铁与碳发生反应的化学方程式
________________________。
(5)实验优化
学习小组有同学认为应对实验装置进一步完善。
①甲同学认为:应将澄清石灰水换成Ba(OH)2溶液,其理由是________________。
②从环境保护的角度,请你再提出一个优化方案将此实验装置进一步完善:________。
查看答案和解析>>
科目: 来源:陕西省模拟题 题型:实验题


查看答案和解析>>
科目: 来源:陕西省模拟题 题型:实验题
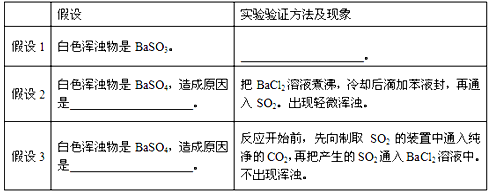
查看答案和解析>>
科目: 来源:陕西省模拟题 题型:实验题
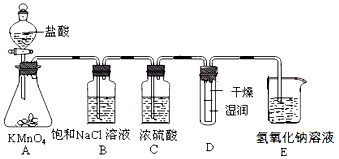
查看答案和解析>>
科目: 来源:模拟题 题型:实验题
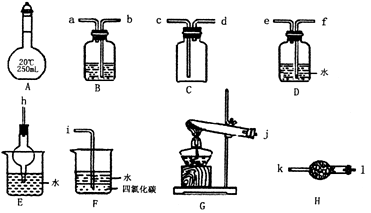
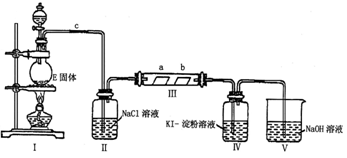
查看答案和解析>>
科目: 来源:陕西省模拟题 题型:实验题

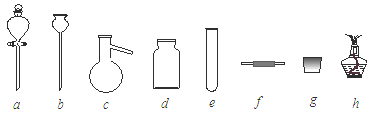
查看答案和解析>>
科目: 来源:模拟题 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com