
科目: 来源: 题型:
随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品氧化变质,在包装袋中可以放入的化学物质是( )
A.无水硫酸铜 B.硫酸亚铁
C.食盐 D.生石灰
查看答案和解析>>
科目: 来源: 题型:
称取两份铝粉,第一份加入足量的NaOH溶液中,第二份加入足量的盐酸中,若放出H2的体积相同(同温同压),则两份铝粉的质量比为( )
A.1:2 B.1:3
C.3:2 D.1:1
查看答案和解析>>
科目: 来源: 题型:
在Fe2(SO4)3、CuSO4和稀H2SO4的混合液中加入Fe粉,反应结束后,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是
A.Fe3+ B.Cu2+
C.Fe2+ D.H+
查看答案和解析>>
科目: 来源: 题型:
除去下列物质中的杂质(括号内是杂质),能采用先与过量NaOH溶液充分反应再过滤的方法的是( )
A.Fe3O4(Al2O3) B.KCl(NaCl)
C.SiO2(CaCO3) D.FeCl2溶液(FeCl3)
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.铜的化学性质活泼,不宜用铜制作盛食品的器皿
B.盛放NaOH溶液的玻璃试剂瓶不能用玻璃塞
C.只用KSCN溶液就可检验FeCl3溶液中的少量Fe2+
D.普通玻璃的组成可用Na2O·CaO·6SiO2表示,是纯净物
查看答案和解析>>
科目: 来源: 题型:
下列有关硅及其化合物的说法错误的是( )
A.硅的导电性能介于导体和绝缘体之间,是良好的半导体材料
B.二氧化硅属于酸性氧化物,不能与任何酸反应
C.硅酸可通过可溶性硅酸盐与其他酸反应制得,硅酸酸性比碳酸弱
D.硅酸钠的水溶液俗称水玻璃,可作木材防火剂
查看答案和解析>>
科目: 来源: 题型:
下列说法中正确的是( )
A.硅是人类将太阳能转变为电能的常用材料
B.工业上镁的制备是电解熔融MgO
C.铝热法制铁适用于野外小范围操作,生物炼铜已经大规模用于铜的生产中
D.海水的各种化学资源的开发过程,必须都要发生化学反应
查看答案和解析>>
科目: 来源: 题型:
铝制品比铁制品在空气中不易被锈蚀,原因是( )
A.铝的密度比铁的密度小
B.铝的金属活动性比铁弱
C.铝在空气中易与氧气反应形成一层致密的氧化膜
D.铝在常温下不与氧气发生化学反应
查看答案和解析>>
科目: 来源: 题型:
1918年,Lewis提出反应速率的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应。能引发化学反应的碰撞称之为有效碰撞。
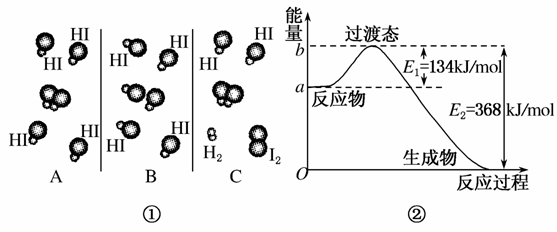
(1)图①是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是________(选填“A”、“B”或“C”)。
(2)20世纪30年代Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。图②是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________________________________________________________
______________________________________________________________。
(3)过渡态理论认为,催化剂改变反应速率的原因是改变了反应的途径,对大多数反应而言主要是通过改变过渡态而导致有效碰撞所需要的能量发生变化。请在图②中作出NO2和CO反应时使用催化剂而使反应速率加快的能量变化示意图。
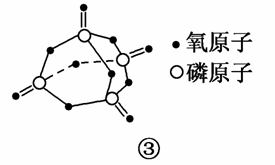
(4)进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键所需吸收的能量,下表是部分化学键的键能数据:
| 化学键 | P—P | P—O | O===O | P===O |
| 键能/kJ·mol-1 | 197 | 360 | 499 | x |
已知白磷的燃烧热为2 378.0 kJ/mol,白磷完全燃烧的产物结构如图③所示,则上表中x=________。
查看答案和解析>>
科目: 来源: 题型:
①CaCO3(s)===CaO+CO2(g) ΔH=177.7 kJ
②C(s)+H2O(s)===CO(g)+H2(g)
ΔH=-131.3 kJ/mol
③H2SO4(l)+NaOH(l)===Na2SO4(l)+H2O(l)
ΔH=-57.3 kJ/mol
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
⑤CO(g)+O2(g)===CO2(g) ΔH=-283 kJ/mol
⑥HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l)
ΔH=-57.3 kJ/mol
⑦2H2(g)+O2(g)===2H2O(l) ΔH=-517.6 kJ/mol
(1)上述热化学方程式中,不正确的有________,不正确的理由分别是_______________________________________________________________。
(2)根据上述信息,写出C转化为CO的热化学方程式_____________。
(3)上述反应中,表示燃烧热的热化学方程式有________________;表示中和热的热化学方程式有________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com