
科目: 来源: 题型:
有人设计以Pt和Zn为电极材料,埋入人体内作为某种心脏病人的心脏起搏器的能源。它依靠跟人体内体液中含有的一定浓度的溶解氧、H+和Zn2+进行工作,试写出该电池的两极反应式。
查看答案和解析>>
科目: 来源: 题型:
以甲烷燃料电池为例来分析在不同的环境下电极反应式的书写方法:
(1)酸性条件
燃料电池总反应式:CH4+2O2 ===CO2+
===CO2+ 2H2O①
2H2O①
燃料电池正极反应式:O2+4H++4e-===2H2O②
①-②×2,得燃料电池负极反应式:__________________________。
(2)碱性条件
燃料电池总反应式:CH4+2O2+2NaOH===Na2CO3+3H2O①
燃料电池正极反应式:O2+2H2O+4e-===4OH-②
①-②×2,得燃料电池负极反应式:_________________________。
(3)固体电解质(高温下能传导O2-)
燃料电池总反应式:CH4+2O2===CO2+2H2O①
燃料电池正极反应式:O2+4e-===2O2-②
①-②×2,得燃料电池负极反应式:_____________________________。
(4)熔融碳酸盐(如:熔融K2CO3)环境下电池总反应式:CH4+2O2===CO2+2H2O。正极电极反应式:O2+2CO2+4e-===2CO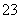 。电池总反应式-正极电极反应式得负极电极反应式:________________________。
。电池总反应式-正极电极反应式得负极电极反应式:________________________。
查看答案和解析>>
科目: 来源: 题型:
铅蓄电池是典型的可充电电池,它的正负极极板是惰性材料,
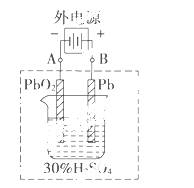
请回答下列问题(不考虑氢、氧的氧化还原):
(1)电解液中H2SO4的浓度将变______________________;
当外电路通过1 mol电子时,理论上负极板的质量增加__________g。
(2)在完全放电耗尽PbO2和Pb时,若按上图连接,电解一段时间后,则在A电极上生成________,B电极上生成____________,此时铅蓄电池的正负极的极性将________。
查看答案和解析>>
科目: 来源: 题型:
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+。下列有关说法正确的是 ( )
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气
C.电池反应的化学方程式为CH3CH2OH+O2===CH3COOH+H2O
D.正极上发生的反应为O2+4e-+2H2O===4OH-
查看答案和解析>>
科目: 来源: 题型:
分析下图所示的四个原电池装置,其中结论正确的是 ( )
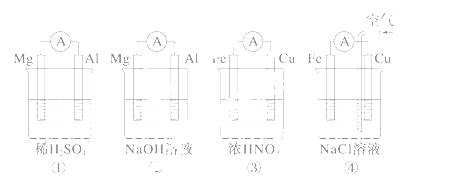
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6H2O+6e-===6OH-+3H2↑
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H2↑
查看答案和解析>>
科目: 来源: 题型:
已知A、B、C为中学化学中常见单质。室温下,A为固体,B和C均为气体。在适宜的条件下,它们有如图所示的转化关系。
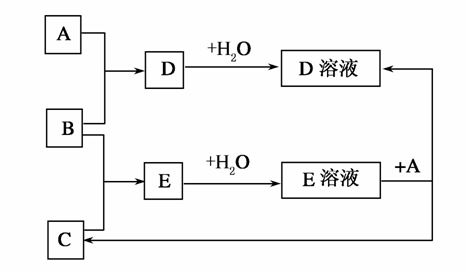
回答下列问题。
(1)A、B、C三种单质的组成元素中的任意两种形成的化合物所属物质类别一定不是________。
①氢化物 ②酸 ③碱 ④盐 ⑤氧化物
理由是_________________________________________。
(2)A、B、C三种元素中有一种是金属,则三种元素中可能是金属的是________,理由是_________________________________。
(3)如果E溶液是一种强酸,写出E作为还原剂参加反应的离子方程式:______________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
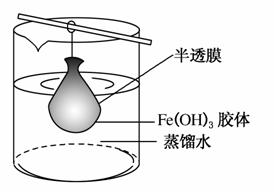
某校课外小组同学制备Fe(OH)3胶体,并研究该胶体的性质。
(1)该小组同学采用了以下操作制备胶体,请将空白处填写完整:
取一个烧杯,加入20 mL蒸馏水,加热至沸腾,然后向烧杯中滴加1 mL~2mL饱和________溶液,继续煮沸,待________后,停止加热。
(2)将制得的胶体放入半透膜制成的袋内,如上图所示,放置2 min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察到________(填写“有”或“无”)丁达尔效应;再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为_____________________________。
(3)若将半透膜内的胶体倒入U形管中,如下图所示,在胶体上方加入少量电解液以保护胶体,接通直流电后,观察到的现象是(填“阴”或“阳”)________极附近颜色逐渐变深,其原因是____________________。

(4)先取上述半透膜内的Fe(OH)3胶体于试管中,逐滴加入稀硫酸,会发生一系列变化。
①先出现红褐色沉淀,原因是__________________________________
______________________________________________________________;
②随后沉淀溶解,该反应的离子方程式是_________________________
______________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊进入患者腹中。明胶是水溶性蛋白质混合物,溶于水形成胶体。由工业明胶制成的胶囊中往往含有超标的重金属Cr,从而对人体造成伤害。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是________价。
(2)化学上可将某些盐写成氧化物的形成,如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成________。
(3)明胶的水溶液和K2SO4溶液共同具备的性质是________。
a.都不稳定,密封放置沉淀
b.两者均会发生丁达尔现象
c.分散质微粒可通过滤纸
(4)已知胶体的分散质不能透过半透膜,但小分子或离子能透过半透膜。现将10 mL明胶的水溶液与5 mL NaBr溶液混合后装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中。若要求只检验一种离子,就能证明Na+、Br-透过半透膜,写出检验该离子的实验方法:________________________。
查看答案和解析>>
科目: 来源: 题型:
化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,不恰当的一种物质是________(填物质名称)。
(2)“三酸”与“两碱”之间均可反应,若用化学方程式表示有六个(酸过量时),若用离子方程式表示却只有两个,请写出这两个离子方程式(酸过量时):
____________________、____________________。
(3)“三酸”常用于溶解金属和金属氧化物,下列块状金属在常温时能全部溶于足量浓硝酸的是________。
A.Au B.Cu
C.Al D.Fe
(4)烧碱、纯碱溶液均可吸收CO2,当含0.1 mol NaOH的溶液吸收一定量CO2后,将溶液低温小心蒸干得到固体的组成可能有四种情况,分别是(填化学式):
①________;②Na2CO3;③________;④NaHCO3
(5)将得到的固体重新溶解于水,向其中加入盐酸,调节溶液的pH恰好等于7,再将溶液蒸干,最终得到固体的质量为________g。
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、W有如图所示的转化关系,则X、Y可能是( )
①C、CO ②AlCl3、Al(OH)3 ③N2、NO ④S、SO2 ⑤NaOH、Na2CO3
A.①②⑤ B.②③⑤
C.③④ D.①②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com