
科目: 来源: 题型:
金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3(s)+3H2(g) W(s)+3H2O(g)
W(s)+3H2O(g)
请回答下列问题:
(1)上述反应的化学平衡常数表达式为________。
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2∶3,则H2的平衡转化率为__________;随温度的升高,H2与水蒸气的体积比减小,则该反应为________反应(填“吸热”或“放热”)。
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温 度 | 25℃~550℃~600℃~700℃ |
| 主要成分 | WO3 W2O5 WO2 W |
第一阶段反应的化学方程式为_____________;
580℃时,固体物质的主要成分为________;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为__________。
(4)已知:温度过高时,WO2(s)转变为WO2(g);
WO2(s)+2H2(g)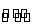 W(s)+2H2O(g) ΔH=+66.0 kJ·mol-1
W(s)+2H2O(g) ΔH=+66.0 kJ·mol-1
WO2(g)+2H2(g)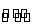 W(s)+2H2O(g) ΔH=-137.9 kJ·mol-1
W(s)+2H2O(g) ΔH=-137.9 kJ·mol-1
则WO2(s)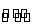 WO2(g)的ΔH=______。
WO2(g)的ΔH=______。
(5)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W(s)+2I2(g)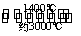 WI4(g)。下列说法正确的有________。
WI4(g)。下列说法正确的有________。
a.灯管内的I2可循环使用
b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
查看答案和解析>>
科目: 来源: 题型:
偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2(l)+2N2O4(l)====2CO2(g)+3N2(g)+4H2O(g)(Ⅰ)
(1)反应(Ⅰ)中氧化剂是________。
(2)火箭残骸中常见红棕色气体,原因为:
N2O4(g)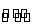 2NO2(g)(Ⅱ)
2NO2(g)(Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为______(填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________。
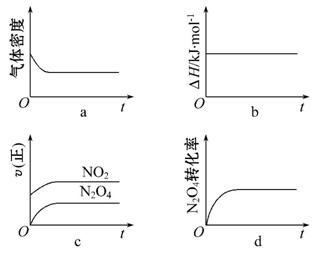
若在相同温度下,上述反应改在体积为1 L的恒容密闭容器中进行,平衡常数______________(填“增大”“不变”或“减小”),反应3 s后NO2的物质的量为0.6 mol,则0~3 s内的平均反应速率v(N2O4)=____________mol·L-1·s-1。
(4)NO2可用氨水吸收生成NH4NO3。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是________(用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将____(填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为________mol·L-1。(NH3·H2O的电离平衡常数取Kb=2×10-5mol·L-1)
查看答案和解析>>
科目: 来源: 题型:
反应A(g)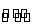 B(g)+C(g)在容积为1.0 L的密闭容器中进行,A的初始浓度为0.050 mol·L-1。温度T1和T2下A的浓度与时间关系如下图所示。回答下列问题:
B(g)+C(g)在容积为1.0 L的密闭容器中进行,A的初始浓度为0.050 mol·L-1。温度T1和T2下A的浓度与时间关系如下图所示。回答下列问题:
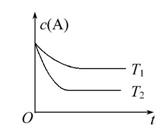
(1)上述反应的温度T1________T2,平衡常数K(T1)________K(T2)。(填“大于”“小于”或“等于”)
(2)若温度T2时,5 min后反应达到平衡,A的转化率为70%,则:
①平衡时体系总的物质的量为________。
②反应的平衡常数K=________。
③反应在0~5 min区间的平均反应速率v(A)=_________。
查看答案和解析>>
科目: 来源: 题型:
已知反应Fe(s)+CO2(g) 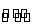 FeO(s)+CO(g)
FeO(s)+CO(g)
ΔH=akJ·mol-1,平衡常数为K。测得在不同温度下,K值如下:
| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
(1)若500℃时进行反应,CO2的起始浓度为2 mol·L-1,CO的平衡浓度为________。
(2)该反应为______(选填“吸热”或“放热”)反应。
(3)700℃时反应达到平衡状态,要使该平衡向右移动,其他条件不变时,可以采取的措施有___________(填序号)。
A.缩小反应器体积 B.通入CO2
C.升高温度到900℃ D.使用合适的催化剂
E.增加Fe的量
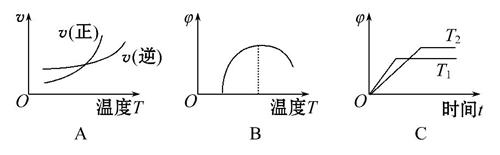
(4)下列图像符合该反应的是______(填序号)(图中v为速率,φ为混合物中CO含量,T为温度且T1>T2)。
查看答案和解析>>
科目: 来源: 题型:
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 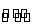 2G(g),忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g),忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
| 压强/MPa体积分数/%温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
①b<f
②915℃、2.0 MPa时E的转化率为60.0%
③该反应的ΔS>0
④K(1 000℃)>K(810℃)
上述①~④中正确的有( )
A.4个 B.3个 C.2个 D.1个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com