
科目: 来源: 题型:
 恒容体系,发生如下反应2A(g)
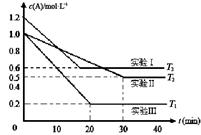
恒容体系,发生如下反应2A(g)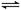 B(g)+xC(g) ΔH,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如右图。某课外活动小组一共进行了如图所示的三个实验(其中T1、T2表示不同的反应温度)。
B(g)+xC(g) ΔH,起始时B、C物质的量浓度为0,A的物质的量浓度随时间变化如右图。某课外活动小组一共进行了如图所示的三个实验(其中T1、T2表示不同的反应温度)。
(1)在实验Ⅲ中,0~20min的时间内,v(A)= 。
(2)分析实验I和实验II的数据,可知x= ;分析实验II和实验Ⅲ的数据,可知反应热ΔH 0(选填“>”、“=”或者“<”)。
(3)能说明该反应达到平衡状态的是(选填代号字母) 。
 a.A的质量不再变化
a.A的质量不再变化
b.混合气体的密度保持不变
c.用A、B、C表示的反应速率的比为2∶1∶x
d.单位时间内生成n mol B的同时生成2n mol A
e.混合气体的平均摩尔质量保持不变
(4)T1℃时,保持容器的体积不变,若充入a mol A、b mol B、c mol C,达到平衡时C的体积分数为0.4,则a、b、c应满足什么条件 。
查看答案和解析>>
科目: 来源: 题型:
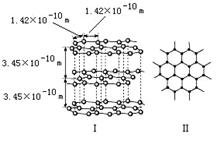
(1)石墨是层状结构,如下图所示。每一层内的碳原子间通过sp2杂化形成 (填代号字母,后同);层与层间存在 ;石墨的每一个碳原子经过sp2杂化后,还剩下1个未成对电子,在电场作用下能够作定向移动,因而石墨还具有导电性,所以还存在 。
a:σ键 b:π键 c:氢键 d:配位键
e:范德华力 f:金属键 g:离子键
(2)请选“>”、“<”或“=”填与下列空格中:
①熔点:Na Mg;②硬度:金刚石 晶体硅;③晶格能:NaI NaBr
查看答案和解析>>
科目: 来源: 题型:
2.0 mol PCl3和1.0 mol Cl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+Cl2(g) PCl5(g) 达平衡时PCl5为0.40 mol,如果此时再加入2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
PCl5(g) 达平衡时PCl5为0.40 mol,如果此时再加入2.0 mol PCl3和1.0 mol Cl2,在相同温度下再达平衡时PCl5的物质的量是
A.小于0.40 mol B.大于0.80 mol
C.等于0.80 mol D.大于0.40 mol,小于0.80 mol
查看答案和解析>>
科目: 来源: 题型:
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g) N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
| A | B | C | D |
|
|
|
|
|
| 升高温度,平衡常数减小 | 0~3s内,反应速率为: v(NO2)=0.2 mol·L-1 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
科目: 来源: 题型:
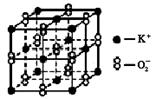
高温下,超氧化钾晶体(KO2)呈立方体结构(与NaCl晶体结构相似)。如图为超氧化钾晶体的一个晶胞。则有关下列说法不正确的是
A.KO2中既存在离子键也存在共价键
B.一个KO2晶胞中摊得的K+和O2-粒子数均为4个
C.晶体中与每个K+距离最近的O2-有8个
D.与K+距离相等且最近的K+有12个
查看答案和解析>>
科目: 来源: 题型:
已知2H2(g)+O2(g)=2H2O(g) ΔH=-484 kJ/mol。且氧气中1 mol O=O键完全断裂时吸收热量496 kJ,水蒸气中1 mol H—O键形成时放出热量463 kJ,则氢气中1 mol H—H键断裂时吸收热量为
A.920 kJ B.557 kJ C.436 kJ D.188 kJ
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是
A.某微粒空间构型为三角锥形,则该微粒一定是极性分子
B.某微粒空间构型为V形,则中心原子一定有孤电子对
C.sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组新轨道
D.凡是中心原子采取sp3杂化轨道成键的分子其立体构型都是正四面体
查看答案和解析>>
科目: 来源: 题型:
某反应:A  B+C 在低温下不能自发进行,在高温下能自发进行,对该反应过程ΔH、ΔS的判断正确的是
B+C 在低温下不能自发进行,在高温下能自发进行,对该反应过程ΔH、ΔS的判断正确的是
A.ΔH<0、ΔS<0 B.ΔH>0、ΔS<0
C.ΔH<0、ΔS>0 D.ΔH>0、ΔS>0
查看答案和解析>>
科目: 来源: 题型:
下列关于中和热测定实验中的叙述不正确的是
A.应用环形玻璃搅拌棒轻轻搅动混合液
B.实验中应使用相同浓度和体积的NaOH和HCl
C.实验中两个大小不同的烧杯间要填满碎纸条,目的是减少实验过程中热量的损失
D.用相同体积的浓硫酸代替HCl溶液进行实验,测得中和热的数值比理论值偏高
查看答案和解析>>
科目: 来源: 题型:
现有三种元素的基态原子的电子排布式如下:① [Ne]3s23p4;② 1s22s22p63s23p3;③1s22s22p5。则上述三种原子的第一电离能大小关系正确的是
A.②>①>③ B.③>①>②
C.③>②>① D.①>②>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com