
科目: 来源:同步题 题型:实验题

查看答案和解析>>
科目: 来源:同步题 题型:实验题

查看答案和解析>>
科目: 来源:同步题 题型:实验题
查看答案和解析>>
科目: 来源:同步题 题型:不定项选择题
查看答案和解析>>
科目: 来源:同步题 题型:实验题

查看答案和解析>>
科目: 来源:同步题 题型:实验题

查看答案和解析>>
科目: 来源:同步题 题型:实验题



(1)该研究性学习小组的实验目的是___。
(2)该研究性学习小组进行实验时所用的方法是科学实验中常用的一种方法,该方法叫____法;
(3)实验(1)得出的结论是____。
(4)由实验(2)和实验(3)得出的结论是(写三点)____,____,____
(5)据有关现象写出草酸溶液与酸性高锰酸钾溶液反应的离子方程式:
___H2C2O4+___MnO4-+____H+==____Mn2++____CO2↑+___H2O
查看答案和解析>>
科目: 来源:福建省高考真题 题型:实验题

查看答案和解析>>
科目: 来源:专项题 题型:实验题
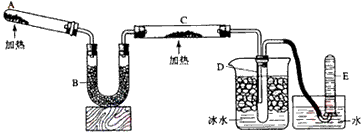
查看答案和解析>>
科目: 来源:山西省模拟题 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com